
使用胆矾(CuSO4·5H2O)配制1 L 0.1 mol·L-1 的硫酸铜溶液,正确的是
A.将胆矾加热除去结晶水后,称取16 g 溶于1 L 水中
B.称取胆矾25 g 溶于1 L水中
C.将25 g 胆矾溶于少量水中,然后将溶液稀释到 1 L
D.将12.5 g 无水CuSO4 溶于水中,然后将此溶液稀释至1 L
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
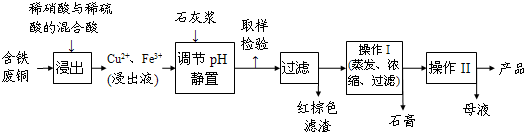
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
科目:高中化学 来源:2010年云南省高一上学期期中检测化学卷 题型:选择题
使用胆矾(CuSO4·5H2O)配制1 L 0.1 mol·L-1 的硫酸铜溶液,正确的是
A.将胆矾加热除去结晶水后,称取16 g 溶于1 L 水中
B.称取胆矾25 g 溶于1 L水中
C.将25 g 胆矾溶于少量水中,然后将溶液稀释到 1 L
D.将12.5 g 无水CuSO4 溶于水中,然后将此溶液稀释至1 L
查看答案和解析>>
科目:高中化学 来源: 题型:
使用胆矾(CuSO4·5H2O)配制1 L 0.1 mol·L-1的硫酸铜溶液,正确的是
A.将胆矾加热除去结晶水后,称取16 g 溶于1 L 水中
B.称取胆矾25 g 溶于1 L水中
C.将25 g 胆矾溶于少量水中,然后将溶液稀释到 1 L
D.将12.5 g 无水CuSO4溶于水中,然后将此溶液稀释至1 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com