
两个化学兴趣小组进行了以下探究活动:
第一组:为研究铁质材料与热浓硫酸的反应,
(1)称取铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为 (选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。据此推知气体Y 中SO2的体积分数为 。
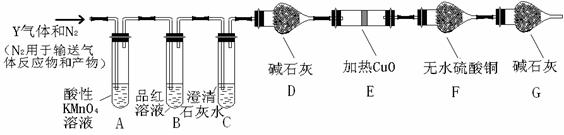 分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
(2)写出产生CO2的化学方程式 。
(3)装置A中试剂的作用是 ,反应的离子方程式 。
(4)简述确认气体Y中含有CO2的实验现象 。
(5)如果气体Y中含有H2,预计实验现象应是 。
 第二组:拟用下列装置定量分析空气中SO2的含量:
第二组:拟用下列装置定量分析空气中SO2的含量:
(6)KMnO4溶液中导管末端做成球状多孔结构的作用是
(7)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为 g/L
科目:高中化学 来源: 题型:
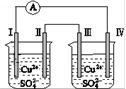
某同学组装了如图所示的电化学装置,电极Ⅰ为Zn,其他电极均为Cu,
则下列说法正确的是( )
 A.电子移动:电极Ⅰ→电极Ⅳ→电极Ⅲ→电极Ⅱ
A.电子移动:电极Ⅰ→电极Ⅳ→电极Ⅲ→电极Ⅱ
B.电极Ⅰ发生还原反应
C.电极Ⅳ逐渐溶解
D.电极Ⅲ的电极反应:Cu-2e-===Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
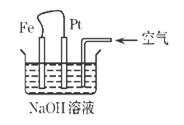
有关右图装置中的叙述正确的是
A.这是电解NaOH溶液的装置
B.这是一个原电池装置
C.Pt为负极,其电极反应为:O2+2H2O+4e-= 4OH-
D.Fe为阳极,其电极反应为:Fe-2e-+2OH- = 2Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
为确定下列置于空气中的物质是否变质,所选检验试剂(括号内)不能达到目的的是( )
A.Na2SO3溶液(BaCl2溶液) B.FeSO4溶液(KSCN溶液)
C.漂白粉(稀硝酸) D.NaOH溶液[Ba(OH)2溶液]
查看答案和解析>>
科目:高中化学 来源: 题型:
蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于
过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是( )
A.沉淀X的成分是SiO2
B.将蛇纹石试样直接溶于过量的NaOH溶液后过滤,得到的不溶物为Fe2O3
C.在溶液Y中加入过量的NaOH溶液,过滤得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
D.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.实验室中的浓硝酸呈现黄色,是因为浓硝酸具有强氧化性
B.澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液
C.NO和NO2密度比空气大,所以均可用向上排空气法收集
D.在海轮外壳上镶入锌块可减缓船体的腐蚀,是利用了原电池的原理
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列各溶液中,一定能大量共存的离子组是 ( )
A.强酸性溶液中:K+、S2-、ClO-、SO42-
B.含有0.1mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3-
C.室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42-
D.加入Al能放出H2的溶液中::Na+、K+、CO32-、Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D中,0.5 mol A元素的离子得到6.02×1023个电子后被还原为中性原子,0.4 g A的氧化物恰好与100 mL 0.2 mol/L的盐酸完全反应,A元素原子核内质子数与中子数相等;B元素原子核外电子数比A元素原子核外电子数多1,C-离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍。请填写下列空格:
(1)A、B、C、D四种元素的符号:A________B________,C________,D________。
(2)C、D两元素组成的物质,分子内含有__________键(填“极性”或“非极性”,下同),其电子式是____________。
(3)A、B、C三种元素的离子半径由大到小的顺序为________________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢
化物可与其最高价含氧酸反应生成离子化合物,由此可知
| W | X | |
| Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com