
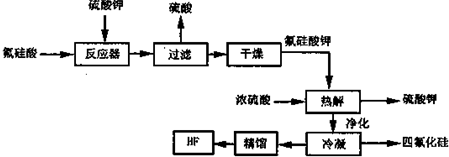
���� �������������ط�����Ӧ���ɷ�����أ�K2SiF6�����ԣ�����ʪ�ԣ�����ˮ�����˵õ�����ͷ�����أ����������ˮ��ˮ��ɷ����ء������⼰���ᣬ����Ũ���ᷴӦ�õ�����ء������⡢�����Ȼ���ȣ�����������ͨ������õ������ķ����⣻
��1���������������ط�����Ӧ���ɷ�����غ����
��2�����ݹ���װ�ú���ѡ����Ҫ�IJ��������������������ˮ�������ڴ���Ϊ������ʧ�������Ҵ�ϴ�ӣ�
��3����Ӧ�����в��뷴Ӧ���ڷ�Ӧ���������������ɵ����ʿ���ѭ��ʹ�ã����������жϣ�
��4����������Ը�ʴ�̻��������ڿ�ʴ����������Ҳ������H2SiF6 ������ԭ���غ���ƽ��д��ѧ����ʽ��
��5���������ɷ����Ƶ������������ʵ��������Ԫ���غ�õ������з���������ʵ���������õ���������������=$\frac{����������}{����������}$��100%������²��2.24L��������Ϊ3.1g�����������ԶԶ����2.0g��ԭ���Ƿ�������Ӽ�����γ���������ֽ���γ�˫���
��� �⣺�������������ط�����Ӧ���ɷ�����أ�K2SiF6�����ԣ�����ʪ�ԣ�����ˮ�����˵õ�����ͷ�����أ����������ˮ��ˮ��ɷ����ء������⼰���ᣬ����Ũ���ᷴӦ�õ�����ء������⡢�����Ȼ���ȣ�����������ͨ������õ������ķ����⣻
��1���������������ط�����Ӧ���ɷ�����غ����ᣬ��Ӧ���еĻ�ѧ����ʽΪ��H2SiF6+K2SO4=H2SO4+K2SiF6����
�ʴ�Ϊ��H2SiF6+K2SO4=H2SO4+K2SiF6����
��2�����ݹ���װ�ú���ѡ����Ҫ�IJ�������Ϊ©�����ձ�������������ϴ�ӷ�����أ�K2SiF6��ʱ���þƾ�ϴ�Ӷ�������ˮ����Ŀ���Ƿ����������ˮ�������ڴ���Ϊ������ʧ���Ҵ�ϴ�ӣ�
�ʴ�Ϊ��©�����ձ�����������������ز����ھƾ���������ˮϴ���ܽ���������ʧ��
��3����Ӧ�����в��뷴Ӧ���ڷ�Ӧ���������������ɵ����ʿ���ѭ��ʹ�ã����������ж������������������ڱ����������Ȳμӷ�Ӧ����������ɣ�����ѭ��ʹ�ã�
�ʴ�Ϊ��H2SO4��K2SO4��
��4����������Ը�ʴ�̻��������ڿ�ʴ����������Ҳ������H2SiF6 ��ˮ������ԭ���غ���ƽ��д��ѧ����ʽΪ��6HF+SiO2=H2SiF6+2H2O��
�ʴ�Ϊ��6HF+SiO2=H2SiF6+2H2O��
��5���������ɷ����Ƶ������������ʵ���=$\frac{5.85g}{78g/mol}$=0.075mol�����Ԫ���غ�õ������з���������ʵ���Ϊ0.075mol��2=0.15mol������õ�HF����=0.15mol��20g/mol=3g����������=$\frac{����������}{����������}$��100%=$\frac{3g}{3.1g}$��100%=97%������²��2.24L��������Ϊ3.1g�����������ԶԶ����2.0g��ԭ���Ƿ�������Ӽ�����γ���������ֽ���γ�˫���
�ʴ�Ϊ��97%��HF���Ӽ��γ���������ֵϳ�˫���壮
���� ��������ʪ��������ĸ���Ʒ�������������������Ĺ���Ϊ������ͨ�����̷�����ʵ�����������������ѡ�����������ʵ�ѭ��ʹ�õȣ��������Ӧ�õ����������������Ϣ�����������ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������˫ԭ�ӷ��� | B�� | ��Ԫ�صķǽ����Ժ�ǿ | ||
| C�� | ��ԭ�ӵİ뾶��С | D�� | �������еĻ�ѧ�������ƻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Ӽ�ͨ�������������γɵĻ�ѧ����Ϊ���Ӽ� | |
| B�� | ��MgO��CO2 �����ж������ڵ������� | |
| C�� | �����д��������ƶ��Ĵ������������ܵ��� | |
| D�� | ���Ӿ����д��ڴ������������ܵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
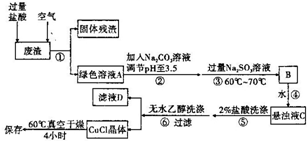 ͨ������£�CuCIΪ��ɫ��ĩ������ˮ���������Ҵ����������л��ϳɵĴ��������������ϡ������ȹ�ҵ��CuCI¶���ڿ����н��ױ�����Ϊ��ɫ�ĸ�ͭ�Σ������ֽ⣬��ɺ�ɫ���ܳ��ױ��������ɫ���л���װ���ڵ���ϳɵ����������У������߷�������������Һ�����й�����Һ�к���Si��Cu���л��赥������ʣ�������Һ����������ɵõ������衢ͭ��̼�ķ�������ͼ�Ǵӷ�������ȡCuCI��һ�ֹ�������ͼ��
ͨ������£�CuCIΪ��ɫ��ĩ������ˮ���������Ҵ����������л��ϳɵĴ��������������ϡ������ȹ�ҵ��CuCI¶���ڿ����н��ױ�����Ϊ��ɫ�ĸ�ͭ�Σ������ֽ⣬��ɺ�ɫ���ܳ��ױ��������ɫ���л���װ���ڵ���ϳɵ����������У������߷�������������Һ�����й�����Һ�к���Si��Cu���л��赥������ʣ�������Һ����������ɵõ������衢ͭ��̼�ķ�������ͼ�Ǵӷ�������ȡCuCI��һ�ֹ�������ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ�ص���Ҫ���ϼ۶���+2�� | |
| B�� | Ԫ�صĵ��ʶ�������ɫ | |
| C�� | �е�Ԫ�صĵ��ʿ�����Ȼ�����ȶ����� | |
| D�� | ���а�������Ϊ��������������Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ƿ���ж��������ѷ�ɢϵ��Ϊ��Һ�����塢��Һ | |
| B�� | ������ˮ��Һ����ۻ�״̬���Ƿ�����ʷ�Ϊ����ʡ��ǵ���� | |
| C�� | ���Ǻ���̼Ԫ�ص�����Ϊ�л������̼Ԫ�ص�����Ϊ���� | |
| D�� | �����ܶȴ�С�ѽ�����Ϊ��������ؽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com