
【题目】铁氧体是一类磁性材料,通式为MO·xFe2O3(M为二价金属离子),如Fe3O4可表示为FeO·Fe2O3,制备流程为:
![]()
根据题意回答:
(1)现称取2.8 g铁粉,加入一定量的稀硫酸使其完全溶解后,再加入_____g的FeCl3固体,经上述反应后,方可得到纯净的Fe3O4;
(2)如果以MgSO4和FeCl3为原料,要获得18.0克MgO·2Fe2O3,在制取过程中至少需要1 mol/L的NaOH溶液____mL;
(3)在一次制备Fe3O4的实验中,由于反应物比例控制不当,获得了另一种产品。取一定量该产品溶于足量盐酸中,还需通入标准状况下672 mLCl2才能把溶液中的Fe2+全部氧化为Fe3+,然后把所得溶液蒸干,灼烧至恒重,得9.6 g固体。该产品的化学式为_______;
(4)有一种在电子工业上应用广泛的含铬铁氧体,其组成可表示为:![]() ,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为___________________。
,现有15.2 g FeSO4,经Cr2O72-、H2O2等物质处理后(不再引入含铁物质),可得到含铬铁氧体的质量范围为___________________。
【答案】 16.25 700 2Fe O ·Fe2O3 (7.73g, 11.4 g)
【解析】(1)2.8g铁粉可得到0.05 mol 的FeSO4,依题意还需要 0.1 mol的FeCl3,即16.25g
(2)18.0克MgO·2Fe2O3为0.05 mol,依据元素守恒可得到分别需要MgSO4和FeCl3为0.05 mol、0.2 mol,两者全部沉淀需要0.7 mol的NaOH,需1 mol/L的NaOH溶液为700 ml
(3)该产品可看出是由FeO和Fe2O3以一定量的比组成
由Fe2+~2Cl2可求出Fe2+的量也就是FeO为0.06 mol;而Fe2+经氧化后再蒸干、灼烧至恒重得9.6 g固体为Fe2O3,其物质的量为0.06 mol,也就是其中铁元素为0.12 mol,其中来自FeO的为0.06 mol,那么Fe2O3的物质的量就为0.03 mol,所以该产品的组成可表示为2FeO·Fe2O3或Fe4O5
(4)15.2 g FeSO4也就是0.1 mol的铁元素,由元素守恒可知,当x=0时,所得含铬铁氧体就是Fe3O4,其质量为116/15g;当x=1时,所得含铁氧体是Fe2CrO4,,其质量为11.4g;


科目:高中化学 来源: 题型:
【题目】下列物质俗名与化学式对应错误的是
A.胆矾 CuSO45H2O
B.重晶石 BaSO3
C.绿矾 FeSO47H2O
D.明矾KAl(SO4)212H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1和图2是A、B两种物质的核磁共振氢谱.请根据图1和图2两种物质的核磁共振氢谱谱图选择出可能属于图1和图2的两种物质的分子式( ) 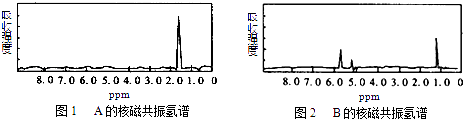
A.A是C3H6、B是C2H6
B.A是C6H6、B是C4H6
C.A是C6H6、B是C2H6
D.A是C3H8、B是C6H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.1mol硫酸铝钾中阴离子所带电荷总数为2NA
B.等质量的乙炔和苯分别完全燃烧,乙炔和苯都消耗7.5NA个氧气分子
C.将0.1mol碳酸钠溶于1L水中,所得溶液含有CO ![]() 和HCO
和HCO ![]() 共0.1NA个
共0.1NA个
D.在H2O2作燃料电池的负极原料时,每摩尔H2O2转移的电子数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液(1)汽油和氯化钠溶液;(2)酒精和水的混合溶液;(3)氯化钠和单质溴的溶液;以上混合溶液分离的正确方法依次是( )
A.分液、萃取、蒸馏B.萃取、蒸馏、分液
C.分液、蒸馏、萃取D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32﹣、SO42﹣、NO3﹣中的几种.①若加入锌粒,会产生H2;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.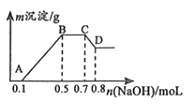
则:
(1)溶液中一定含有的阳离子有 , 一定不含有的离子有 .
(2)C→D的离子方程式为 .
(3)由A→B及C→D段有关数据可计算出的某两种离子的物质的量浓度分别为molL﹣1和molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在常温下,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是( ) 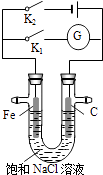
A.K1闭合,铁棒上发生的反应为2H++2e﹣═H2↑
B.K1闭合,石墨棒周围溶液pH逐渐降低
C.K2闭合,铁棒不易被腐蚀,电路中通过0.001NA个电子时,摇匀后溶液的pH为11
D.K2闭合,电路中通过0.002 NA个电子时,两极共产生0.002mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(反应条件及副产物已略去)。
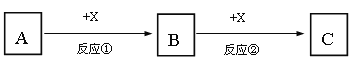
(1)若A、B、C均为含有同种非金属元素的化合物,A为使湿润的红色石蕊试纸变蓝的气体,B接触空气立刻变为C,则反应①的化学方程式为_______________________。
(2)若A、B、C为焰色反应均呈黄色的化合物,X为无色无味气体,则反应②的离子方程式为_____________________________________________。
(3)若A、B、C均为含有同种金属元素的化合物,X是强碱,则反应②的离子方程式为________________________________________________。
(4)若A为单质Fe,X为稀硝酸,则反应②的离子方程式为___________________;若向B的溶液中加入氢氧化钠溶液,现象为________________________________________,对应的化学方程式为___________________________________________。
(5)若A和X均为单质,B为可使品红溶液褪色的气体,则反应②的化学方程式为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com