
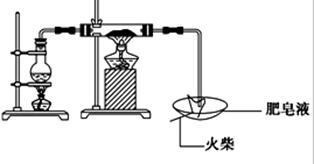
| | 实验步骤 | 预期现象与结论 |
| 步骤1 | 取反应后干燥的固体ag于试管中,加入足量的1mol/L CuSO4溶液,充分振荡,经固液分离、洗涤后,再向固体中滴加足量的 ,振荡溶解,过滤后将滤液配成250mL溶液,待用。 | |
| 步骤2 | 取少量步骤1中滤液于试管中, | |
| 步骤3 | 取少量步骤1中滤液于试管中, | |
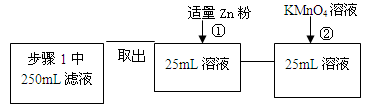
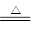 Fe3O4+4H2(2分)
Fe3O4+4H2(2分)| | 实验步骤 | 预期现象与结论 |
| 步骤1 | 3mol/L H2SO4(2分) | |
| 步骤2 | 滴加1~2滴20%KSCN(2分) | 溶液变红色,则固体产物含+3价铁(1分) |
| 步骤3 | 滴加1~2滴0.01mol/L KMnO4(2分) | 溶液紫色褪去,则固体产物含+2价铁(1分) |
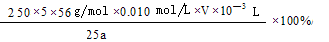 (2分)
(2分)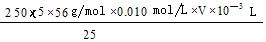 ,再求质量分数即可
,再求质量分数即可

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.Fe3+、Cu2+ | B.Fe2+、Al3+ | C.Fe3+、Al3+ | D.Fe2+、Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 温度/0C | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| NaClO浓度/mol·L-1 | 4.6 | 5.2 | 5.4 | 5.5 | 4.5 | 3.5 | 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若无固体剩余,则溶液中一定有Fe3+ |
| B.若有固体存在,则溶液中一定有Fe2+ |
| C.若溶液中有Cu2+,则一定没有固体析出 |
| D.若溶液中有Fe2+,则一定有Cu析出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |

 R2Cu(有机相)+ 2H+(水相)
R2Cu(有机相)+ 2H+(水相)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeCl3 | B.HNO3 | C.HCl | D.KNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com