
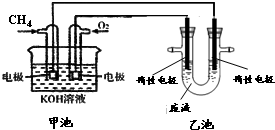
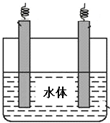
 氯化铁溶液常作印刷电路铜板的腐蚀剂,得 到含有Cu2+等的废液,有人提出可以利用如图的装置从得到的废液中提炼金属铜.该过程中甲池负极的电极反应式是CH4+10OH--8e-=CO32-+7H2O,若乙池中装入废液500mL,当阴极增重3.2g时,停止通电,此时阳极产生气体的体积(标准状况)为1.12L(假设气体全部逸出).
氯化铁溶液常作印刷电路铜板的腐蚀剂,得 到含有Cu2+等的废液,有人提出可以利用如图的装置从得到的废液中提炼金属铜.该过程中甲池负极的电极反应式是CH4+10OH--8e-=CO32-+7H2O,若乙池中装入废液500mL,当阴极增重3.2g时,停止通电,此时阳极产生气体的体积(标准状况)为1.12L(假设气体全部逸出). 分析 甲池是甲烷燃料电池,燃料失电子在负极发生氧化反应,乙池为电解池,依据电路中电子守恒结合电极反应计算.
解答 解:通入甲烷的一端为原电池的负极失电子发生氧化反应,电极反应为:CH4+10OH--8e-=CO32-+7H2O,若乙池中装入废液500mL,得到的废液中提炼金属铜,阴极电极反应为:Cu2++2e-=Cu,当阴极增重3.2g是铜物质的量为0.05mol,电子转移为0.1mol,停止通电,阳极电极反应氯离子失电子生成氯气,电极反应2Cl--2e-=Cl2↑,此时阳极产生气体的体积为0.05mol,标准状况下体积=0.05mol×22.4L/mol=1.12L;
故答案为:CH4+10OH--8e-=CO32-+7H2O;1.12L.
点评 本题考查了原电池电极反应和电解原理的应用和计算,题目难度中等,注意燃料电池工作原理规律是关键.


科目:高中化学 来源: 题型:选择题
 有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):NN键为942、O=O键为500、O-H键为463,则断裂1mol N-H键所需的能量是( )
有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):NN键为942、O=O键为500、O-H键为463,则断裂1mol N-H键所需的能量是( )| A. | 658 | B. | 516 | C. | 391 | D. | 194 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
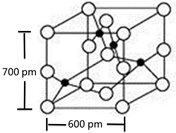 X、Y、M、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子.请回答下列问题:
X、Y、M、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子.请回答下列问题: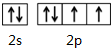 ;Z所在周期中第一电离能最大的主族元素是氯(元素名称)
;Z所在周期中第一电离能最大的主族元素是氯(元素名称)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加Ni的量可提高CO的转化率,Ni的转化率降低 | |
| B. | 缩小容器容积,平衡右移,△H减小 | |
| C. | 反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低 | |
| D. | 当4v正[Ni(CO)4]=v正(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
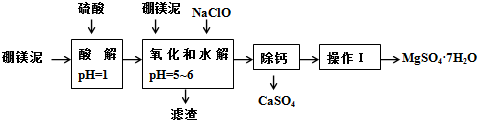
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com