
| A. | ①④ | B. | ②④ | C. | ③⑤ | D. | ④⑥ |
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸或与水、所有中和反应、绝大多数化合反应、铝热反应;
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气)还原金属氧化物、某些复分解(如铵盐和强碱).
解答 解:①液态水汽化需要吸收热量,属于物理变化;
②苛性钠溶于水 过程中放热,溶解是物理变化;
③将胆矾加热变为白色粉末是硫酸铜晶体失去结晶水属于吸热反应;
④生石灰跟水反应生成熟石灰是氧化钙和水反应生成氢氧化钙的化合反应属于放热反应;
⑤氯酸钾分解制氧气是加热才能持续进行的吸热反应;
⑥干冰升华需要吸收能量属于物理变化;
故选C.
点评 本题考查吸热反应,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 目的 | 实验室制O2 | 配置稀硫酸溶液 | 在铁制品上镀铜 | 检查装置气密性 |
| 装置或操作 | 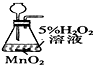 | 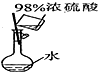 | 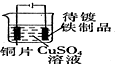 | 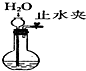 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ②
②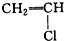 ③
③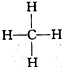 ④
④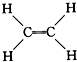 ⑤CH3CH2OH,⑥C6H12O6,⑦CH3COOH,⑧硬脂酸甘油酯,⑨聚乙烯
⑤CH3CH2OH,⑥C6H12O6,⑦CH3COOH,⑧硬脂酸甘油酯,⑨聚乙烯| A. | 能与溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑨ | |
| B. | 投入钠能产生H2的是⑤⑦⑧ | |
| C. | 属于高分子材料的是⑧⑨ | |
| D. | 既能和NaOH溶液反应又能与NaHCO3溶液反应的是 ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 10种 | C. | 12种 | D. | 多于12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
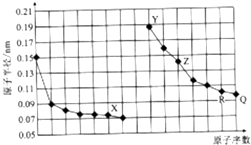
| A. | QX2、RX2都有杀菌消毒的作用,二者常用于自来水消毒 | |
| B. | 简单离子的半径:X>Y>Z | |
| C. | Y、Z、R对应的最高氧化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
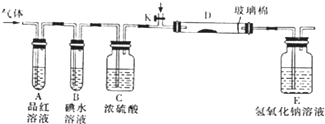
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | ||
| Z |
| A. | X元素的最外层电子数为2 | B. | Y的气态氢化物的化学式为HY | ||
| C. | Z的最高价氧化物的化学式为ZO2 | D. | X、Y、Z的单质中X单质最稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com