

·ÖĪö ¼×”¢¶””¢Īģ·Ö±šŹĒ¼×Ķ锢¶”Ķ锢ĪģĶéµÄĒņ¹÷Ä£ŠĶ£¬ŅŅ”¢±ū·Ö±šŹĒŅŅĶéŗĶ¼×ĶéµÄ±ČĄżÄ£ŠĶ£»
£Ø1£©øł¾Ż±ČĄżÄ£ŠĶ±ķŹ¾µÄŹĒŌ×ÓµÄĻą¶Ō“󊔼°Į¬½ÓŠĪŹ½Ą“½ā“š£¬Ēņ¹÷Ä£ŠĶŹĒĄūÓƶĢĻß“śĢęĘä¹²¼Ū¼ü£»
£Ø2£©Ķ¬Ņ»ÖÖÓŠ»ś»ÆŗĻĪļµÄ½į¹¹ĻąĶ¬£¬±ķŹ¾·½Ź½æÉŅŌ²»Ķ¬£»
£Ø3£©øł¾ŻĶéĢžÖŠĢ¼Ō×ÓŹżÄæ”Ü3µÄĶéĢž²»“ęŌŚĶ¬·ÖŅģ¹¹ĢåĻÖĻ󣬓Ӷ”ĶéæŖŹ¼²Å³öĻÖĶ¬·ÖŅģ¹¹ĻÖĻó£¬øł¾ŻĢ¼Į“Ņģ¹¹ŹéŠ“Ķ¬·ÖŅģ¹¹Ģ壻
£Ø4£©ĶéĢžµÄĶØŹ½ĪŖCnH2n+2£¬ĖęnÖµŌö“ó£¬Ģ¼ŌŖĖŲµÄÖŹĮæ°Ł·Öŗ¬ĮæÖš½„Ōö“ó£»
£Ø5£©C10H14µÄ±½µÄĶ¬ĻµĪļ£¬²ąĮ“ĪŖĶ黳£¬
¢Ł±½»·ÉĻÖ»ŗ¬1øö²ąĮ“£¬Ōņ²ąĮ“ĪŖ-C4H9£¬ĒŅĮ¬½Ó±½»·µÄCŌ×ÓÉĻŗ¬ÓŠHŌ×Ó£¬ĖłŅŌֻŊ¶Ļ¶”ĶéĶ黳µÄĶ¬·ÖŅģ¹¹Ģ弓æÉ£»
¢Ś4øöĢ¼Ō×ÓŠĪ³É2øöČ”“ś»ł£¬Ņ»øöĢ¼Ō×ÓŅ»¶ØŹĒ¼×»ł£¬Į½øöĢ¼Ō×ÓŅ»¶ØŹĒŅŅ»ł£¬ČżøöĢ¼Ō×ÓæÉÄÜŹĒ-CH2CH2CH3 »ņ-CH£ØCH3£©2£¬Į½øöČ”“ś»łĮ¬ŌŚ±½»·ÉĻæÉÄÜÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĒéæö£»
¢Ū4øöĢ¼Ō×ÓŠĪ³É3øöČ”“ś»ł£¬3øöČ”“ś»łĪŖ¼×»ł”¢¼×»ł”¢ŅŅ»ł£¬²ÉČ”¶ØĮ½øö¼×»łµÄĪ»ÖĆ£¬ŅʶÆŅŅ»ł£¬¾Ż“ĖŹéŠ“Ņģ¹¹ĢåÅŠ¶Ļ£»
¢Ü4øöĢ¼Ō×ÓŠĪ³É4øöČ”“ś»ł£¬ŌņČ”“ś»łÖ»ÄÜĪŖ¼×»ł£®
½ā“š ½ā£ŗ£Ø1£©ŅŅ”¢±ūÄܱķŹ¾µÄŹĒŌ×ÓµÄĻą¶Ō“󊔼°Į¬½ÓŠĪŹ½£¬ŹōÓŚ±ČĄżÄ£ŠĶ£»
¹Ź“š°øĪŖ£ŗŅŅ”¢±ū£»
£Ø2£©¼×”¢±ū·Ö±šŹĒ¼×ĶéµÄĒņ¹÷Ä£ŠĶÓė±ČĄżÄ£ŠĶ£¬ŹōÓŚĶ¬Ņ»ÖÖÓŠ»ś»ÆŗĻĪļ£»
¹Ź“š°øĪŖ£ŗ¼×”¢±ū£»
£Ø3£©“ęŌŚĶ¬·ÖŅģ¹¹ĢåµÄŹĒĪģ£ØĪģĶ飩£¬ĘäĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½CH3CH2CH2CH2CH3”¢CH3CH£ØCH3£©CH2CH3”¢C£ØCH3£©4£»
¹Ź“š°øĪŖ£ŗĪģ£»CH3CH2CH2CH2CH3”¢CH3CH£ØCH3£©CH2CH3”¢C£ØCH3£©4£»
£Ø4£©ĶéĢžµÄĶØŹ½ĪŖCnH2n+2£¬ĖęnÖµŌö“ó£¬Ģ¼ŌŖĖŲµÄÖŹĮæ°Ł·Öŗ¬ĮæÖš½„Ōö“ó£¬ŗ¬Ģ¼Įæ×īµĶµÄŹĒ¼×Ķ飬ŗ¬ĒāĮæ×īµĶµÄ·Ö×ÓŹĒĪģĶ飬ĒāŌŖĖŲµÄÖŹĮæ°Ł·Öŗ¬ĮæŹĒ
$\frac{12}{60+12}$”Į100%=16.7%£»
¹Ź“š°øĪŖ£ŗ¼×”¢±ū£»16.7%£»
£Ø5£©C10H14µÄ±½µÄĶ¬ĻµĪļ£¬²ąĮ“ĪŖĶ黳£¬
¢Ł±½»·ÉĻÖ»ŗ¬1øö²ąĮ“£¬Ōņ²ąĮ“ĪŖ-C4H9£¬ĒŅĮ¬½Ó±½»·µÄCŌ×ÓÉĻŗ¬ÓŠHŌ×Ó£¬¶”ĶéĶ黳µÄĢ¼Į“Ķ¬·ÖŅģ¹¹ĢåÓŠ£ŗ £¬¹²4ÖÖ½į¹¹£»
£¬¹²4ÖÖ½į¹¹£»
¢Ś4øöĢ¼Ō×ÓŠĪ³É2øöČ”“ś»ł£¬Ņ»øöĢ¼Ō×ÓŅ»¶ØŹĒ¼×»ł£¬Į½øöĢ¼Ō×ÓŅ»¶ØŹĒŅŅ»ł£¬ČżøöĢ¼Ō×ÓæÉÄÜŹĒ-CH2CH2CH3 »ņ-CH£ØCH3£©2£¬µŚŅ»ĄąĮ½øöČ”“ś»ł·Ö±šĪŖ
¼×»łŗĶ-CH2CH2CH3 »ņ-CH£ØCH3£©2£¬ĖüĆĒĮ¬½ÓŌŚ±½»·ÉĻÓÖÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĒéæö£¬¹²ÓŠ6ÖÖ½į¹¹£¬µŚ¶žĄąĮ½øöČ”“ś»ł¾łĪŖŅŅ»ł£¬ĖüĆĒĮ¬½ÓŌŚ±½»·ÉĻÓÖÓŠĮŚ”¢¼ä”¢¶ŌČżÖÖĒéæö£¬¹²ÓŠ3ÖÖ½į¹¹£¬Ōņ×ܹ²9ÖÖ½į¹¹£»
¢Ū4øöĢ¼Ō×ÓŠĪ³É3øöČ”“ś»ł£¬3øöČ”“ś»łĪŖ¼×»ł”¢¼×»ł”¢ŅŅ»ł£¬²ÉČ”¶ØĮ½øö¼×»łµÄĪ»ÖĆ£¬ŅʶÆŅŅ»ł£¬
ČōĮ½øö¼×»łĪŖĮŚĪ»Ī»ÖĆ£¬¼“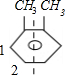 £¬ĪŖ¶Ō³Ę½į¹¹£¬ŅŅ»łÓŠČēĶ¼ĖłŹ¾µÄ2ÖÖČ”“śĪ»ÖĆ£¬ÓŠ2ÖÖ½į¹¹£»
£¬ĪŖ¶Ō³Ę½į¹¹£¬ŅŅ»łÓŠČēĶ¼ĖłŹ¾µÄ2ÖÖČ”“śĪ»ÖĆ£¬ÓŠ2ÖÖ½į¹¹£»
ČōĮ½øö¼×»łĪŖ¼äĪ»Ī»ÖĆ£¬¼“ £¬ĪŖ¶Ō³Ę½į¹¹£¬ŅŅ»łÓŠČēĶ¼ĖłŹ¾µÄ3ÖÖČ”“śĪ»ÖĆ£¬ÓŠ3ÖÖ½į¹¹£»
£¬ĪŖ¶Ō³Ę½į¹¹£¬ŅŅ»łÓŠČēĶ¼ĖłŹ¾µÄ3ÖÖČ”“śĪ»ÖĆ£¬ÓŠ3ÖÖ½į¹¹£»
ČōĮ½øö¼×»łĪŖ¶ŌĪ»Ī»ÖĆ£¬¼“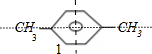 £¬ĪŖ¶Ō³Ę½į¹¹£¬ŅŅ»łÓŠČēĶ¼ĖłŹ¾µÄ1ÖÖČ”“śĪ»ÖĆ£¬ÓŠ1ÖÖ½į¹¹£®
£¬ĪŖ¶Ō³Ę½į¹¹£¬ŅŅ»łÓŠČēĶ¼ĖłŹ¾µÄ1ÖÖČ”“śĪ»ÖĆ£¬ÓŠ1ÖÖ½į¹¹£®
¹²ÓŠ6ÖÖ½į¹¹£»
¢Ü4øöĢ¼Ō×ÓŠĪ³É4øöČ”“ś»ł£¬ŌņČ”“ś»łÖ»ÄÜĪŖ¼×»ł£¬¹²Óė3ÖÖ½į¹¹£¬1£¬2£¬3£¬4-Ėļ׻ł±½”¢1£¬2£¬3£¬5-Ėļ׻ł±½ŗĶ1£¬2£¬3£¬6-Ėļ׻ł±½£¬¹²ÓŠ3ÖÖ½į¹¹£»
ĖłŅŌŹōÓŚ±½µÄĶ¬ĻµĪļµÄĖłÓŠĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ22ÖÖ£»
¹Ź“š°øĪŖ£ŗ22£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļ·Ö×ӵıȥżÄ£ŠĶ”¢Ēņ¹÷Ä£ŠĶ£¬Ķ¬·ÖŅģ¹¹ĢåµČ£¬Ń§ÉśĄūÓĆÄ£ŠĶµĆ³öÓŠ»śĪļµÄ½į¹¹¼ņŹ½ŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬ÕĘĪÕÖ§Į“µÄ½į¹¹ŹĒČ·¶ØĶ¬·ÖŅģ¹¹ĢåµÄ¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
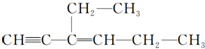 ·Ö×ÓÖŠ“¦ÓŚĖÄĆęĢå½į¹¹ÖŠŠÄµÄĢ¼Ō×ÓŹżĪŖa£¬Ņ»¶Ø“¦ŌŚĶ¬Ņ»Ę½ĆęÄŚµÄĢ¼Ō×ÓŹżĪŖb£¬Ņ»¶Ø“¦ŌŚĶ¬Ņ»Ö±ĻßÉĻµÄĢ¼Ō×ÓŹżĪŖc£¬Ōņa”¢b”¢cŅĄ“ĪĪŖ£Ø””””£©
·Ö×ÓÖŠ“¦ÓŚĖÄĆęĢå½į¹¹ÖŠŠÄµÄĢ¼Ō×ÓŹżĪŖa£¬Ņ»¶Ø“¦ŌŚĶ¬Ņ»Ę½ĆęÄŚµÄĢ¼Ō×ÓŹżĪŖb£¬Ņ»¶Ø“¦ŌŚĶ¬Ņ»Ö±ĻßÉĻµÄĢ¼Ō×ÓŹżĪŖc£¬Ōņa”¢b”¢cŅĄ“ĪĪŖ£Ø””””£©| A£® | 4”¢5”¢3 | B£® | 4”¢6”¢3 | C£® | 2”¢4”¢5 | D£® | 4”¢4”¢6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe3+ | B£® | HS- | C£® | HCO3- | D£® | C6H5O- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4”¢C2H6”¢C3H4 | B£® | C2H6”¢C3H6”¢C4H6 | C£® | CH4”¢C2H6”¢C3H8 | D£® | C2H4”¢C2H6”¢C2H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »Æѧ·“Ó¦ÖŠÓŠĪļÖŹ±ä»ÆŅ²ÓŠÄÜĮæ±ä»Æ | |
| B£® | »Æѧ¼ü¶ĻĮŃĪüŹÕÄÜĮ棬»Æѧ¼üÉś³É·Å³öÄÜĮæ | |
| C£® | ŠčŅŖ¼ÓČȵĻÆѧ·“Ó¦²»Ņ»¶ØŹĒĪüČČ·“Ó¦ | |
| D£® | Ķ¼ĖłŹ¾µÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦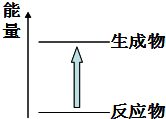 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 168 mL | B£® | 224 mL | C£® | 336 mL | D£® | 504 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
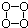 £©£¬ÓŠ¹ŲO4µÄĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
£©£¬ÓŠ¹ŲO4µÄĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | O4µÄĦ¶ūÖŹĮæŹĒ64g | |
| B£® | O4ŗĶO2»„ĪŖĶ¬Ī»ĖŲ | |
| C£® | ĻąĶ¬ÖŹĮæµÄO4ÓėO3Ėłŗ¬Ō×ÓøöŹż±ČĪŖ4£ŗ3 | |
| D£® | O4ÓėO3”¢O2¶¼ŹĒŃõŌŖĖŲµÄĶ¬ĖŲŅģŠĪĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | bŗĶcŹĒĶ¬·ÖŅģ¹¹Ģå | B£® | aŗĶdŹĒĶ¬·ÖŅģ¹¹Ģå | ||
| C£® | aŗĶd¶¼ÄÜ·¢Éś¼Ó³É·“Ó¦ | D£® | Ö»ÓŠbŗĶcÄÜ·¢ÉśČ”“ś·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com