
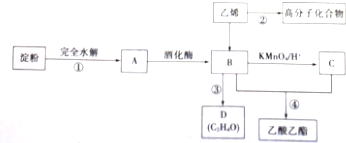
���� ��1-4�����۷�����Ӧ��ˮ�ⷴӦ����AΪ�����ǣ��������ڴ���������ת��ΪB��B�ܱ����������������C����B��C������Ӧ�ܷ�Ӧ����������������BΪCH3CH2OH��CΪCH3COOH��������ϩ������Ӧ�ڼ��Ӿ۷�Ӧ���ɸ߷��ӻ�����Ϊ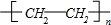 ���ݴ˽��
���ݴ˽��
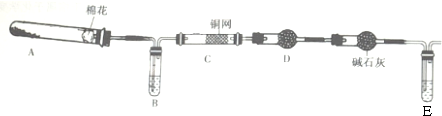
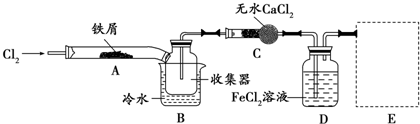
��5����װ��Ϊ�Ҵ���������ʵ��װ�ã�װ���У�װ��A�Ʊ�������װ��B�ṩ�Ҵ�������װ��C���Ҵ������������ڴ��������·���������Ӧ������ȩ��ˮ��D�����ð�ɫ����ˮ����ͭ����ɫ��ĩ��ˮ����ͭ��ˮ����ɫ����ˮ�����ɣ��������ʢ�м�ʯ�ң���ֹE�е�ˮ��������Ӳ�ʲ������У�����C����ʵ�飬װ��Eͨ�����Ƶ�������ͭ����Һ�м��ȳ���ש��ɫ����������ȩ�����ɣ��Դ˽����⣮
��� �⣺��1�����۷�����Ӧ��ˮ�ⷴӦ����AΪ�����ǣ�������A���������ŵ�������ȩ�����ǻ����ʴ�Ϊ��ȩ�����ǻ���
��2����Ӧ��Ϊ��ϩ�����Ӿ۷�Ӧ���ɸ߷��ӻ�����Ϊ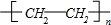 ����ø߷��ӻ������������-CH2-CH2-���ʴ�Ϊ��-CH2-CH2-��
����ø߷��ӻ������������-CH2-CH2-���ʴ�Ϊ��-CH2-CH2-��
��3����Ӧ��Ϊ�������Ҵ���Ũ������������·���������Ӧ��������������ˮ����ѧ����ʽΪCH3COOH+C2H5OH$?_{��}^{Ũ����}$CH3COOCH2CH3+H2O����Ӧ����Ϊ������Ӧ���ʴ�Ϊ��CH3COOH+C2H5OH$?_{��}^{Ũ����}$CH3COOCH2CH3+H2O��������Ӧ��
��4���������Ϸ�����CΪCH3COOH�������������뱥��̼������Һ��Ӧ��������ˮ�����Σ��Ӷ��ﵽ�����������ֲ㣬�ٷ�Һ���ɣ����Գ�ȥ������������������C�IJ�������Ϊ���ѻ��������Һ©���У��ټ��뱥��̼������Һ����������á���Һ��ȡ�ϲ�Һ̬���ʴ�Ϊ���ѻ��������Һ©���У��ټ��뱥��̼������Һ����������á���Һ��ȡ�ϲ�Һ̬��
��5����װ��A�������ķ���װ�ã���A�е�ҩƷ��һ�ִ���������ü���KMnO4�������������仯ѧʽΪKMnO4���ʴ�Ϊ��KMnO4��
��Ӳ�ʲ�����C���Ҵ������������ڴ��������·���������Ӧ������ȩ��ˮ��������Ӧ�Ļ�ѧ����ʽΪ2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O���ʴ�Ϊ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��װ��C���Ҵ������������ڴ��������·���������Ӧ������ȩ��ˮ��װ��Eͨ�����Ƶ�������ͭ����Һ�м��ȳ���ש��ɫ����������ȩ�����ɣ���D��������ˮ����ͭ����ɫ��ĩ��ˮ����ͭ��ˮ����ɫ����ˮ�����ɣ�����D���Լ�Ϊ��ˮ����ͭ���ʴ�Ϊ����ˮ����ͭ��
���� ���⿼�����л����ƶϺ�ʵ�鷽����Ʒ������漰�ǡ�ϩ��������ȩ������������ת����������ѧ���ķ�����ʵ�������Ŀ��飬ע�����ʵ�������жϣ���Ӧԭ����Ӧ�ã������������ʺ�ʵ����������ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʦ���и߶���10���¿���ѧ���������棩 ���ͣ������
������Ҫ���л�����ԭ�ϡ�һ�������£��״���ͬʱ��������������Ӧ��
i .2CH3OH��g�� CH3OCH3��g����H2O��g��
CH3OCH3��g����H2O��g��
ii.2CH3OH��g�� C2H4��g����2H2O��g��
C2H4��g����2H2O��g��
I��������Ӧ�����������仯��ͼ��ʾ��
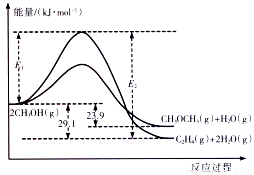
��1����ij�ܱ������У�����һ����CH3OH��g����������������Ӧ����Ӧ________���i����ii���������ʽϴ���ԭ��Ϊ___________�����������м��������ʹii�ķ�Ӧ����������E1��E2-E1�ı仯�ǣ�E1__________��E2��E1___________�����������С�����䡱����
��2����֪��CH3CH2OH��g��=CH3OCH3��g�� ?��H =��50.7 kJ��mol��1������ϩ����ֱ��ˮ�Ϸ�ӦC2H4��g����H2O��g��=C2H5OH��g���Ħ�H= ��
��3�������ݻ�Ϊ2 L�ĺ����ܱ������з���i ��ii��Ӧ������ʼͶ��Ϊ2 mol CH3OH��g�� ��������Ϊ80%ʱ�����������ƽ����Է�������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʦ���и߶���10���¿���ѧ���������棩 ���ͣ�ѡ����
�����йص��жϻ��ʾ������ȷ����
A��һ�������£���0.5 mol N2��g����1.5 mol H2��g�������ܱյ������г�ַ�Ӧ����NH3��g��������19.3 kJ�����Ȼ�ѧ����ʽΪ��N2��g����3H2��g�� 2NH3��g�� ��H����38.6 kJ��mol��1
2NH3��g�� ��H����38.6 kJ��mol��1
B���к��ȵIJⶨʵ������Ҫ�õ���Ҫ����������������С��ͬ���ձ���������С��ͬ����Ͳ���¶ȼơ����β����������Ҳ�����ñ��±������ձ����й��к��Ȳⶨ��ʵ�顣
C���ڲⶨ�к��ȵ�ʵ���У�������Ҫ�ⶨ����¼���¶���3��
D��CO��g����ȼ������283.0 kJ��mol��1����CO2�ֽ���Ȼ�ѧ����ʽΪ��2CO2��g��===2CO��g����O2��g�� ��H����283.0 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
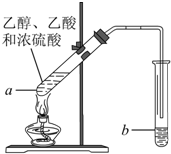 �����Ѿ��ܷⴢ��ʱ��Խ��������Խ�ã�ԭ��֮һ�Ǵ������������������ζ��������ʵ����Ҳ��������ͼ��ʾ��װ����ȡ������������ش��������⣮
�����Ѿ��ܷⴢ��ʱ��Խ��������Խ�ã�ԭ��֮һ�Ǵ������������������ζ��������ʵ����Ҳ��������ͼ��ʾ��װ����ȡ������������ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
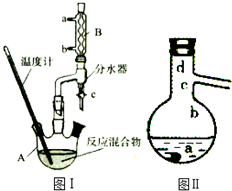 ������������ҽҩ�ϳɵ���Ҫ�м��壬ijͬѧ��ʵ�����������������������ȡ��ʵ��������£�
������������ҽҩ�ϳɵ���Ҫ�м��壬ijͬѧ��ʵ�����������������������ȡ��ʵ��������£�| ������ | ��Է������� | �ܶ�/��g•mL-1�� | �е�/�� | �ܽ�ȣ�g��/��100gˮ�� |
| ������ | 74 | 0.80 | 118.0 | 9 |
| ���� | 60 | 1.045 | 118.1 | ���� |
| ���������� | 1 1 6 | 0.882 | 126.1 | 0.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
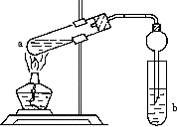 ��ͼ�����Թ�a���ȼ���2mL95%���Ҵ����ټ���3mL��ˮ���ᣬ��ҡ��������2mLŨH2SO4���ò�������ֽ�����Թ̶ܹ�������̨�ϣ����Թ�b�м���7mL����̼������Һ�����Ӻ�װ�ã��þƾ��ƶ��Թ�a���ȣ����۲쵽�Թ�b������������ʱֹͣʵ�飮
��ͼ�����Թ�a���ȼ���2mL95%���Ҵ����ټ���3mL��ˮ���ᣬ��ҡ��������2mLŨH2SO4���ò�������ֽ�����Թ̶ܹ�������̨�ϣ����Թ�b�м���7mL����̼������Һ�����Ӻ�װ�ã��þƾ��ƶ��Թ�a���ȣ����۲쵽�Թ�b������������ʱֹͣʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com