
【题目】下列四种粒子的结构示意图中,说法正确的是
① ②
② ③
③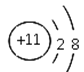 ④
④
A. 它们表示四种不同的元素B. ①④表示的是阳离子
C. ①③④表示的元素都是非金属元素D. ②表示的元素在化合物中通常显+2价
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】已知2H2O(g)=2 H2(g)+O2(g) ΔH=+496kJ·mol-1 。断开1 mol H—H键、O=O键分别需要吸收436 kJ、498 kJ的热量,则断开1 molO—H键需要吸收的热量为( )
A. 462 kJB. 469 kJC. 362 kJD. 466.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要配制2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
A.950 mL,111.2 gB.500 mL,117 g
C.1 000 mL,117 gD.任意规格,111.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质:
A 金刚石与石墨;B 淀粉与纤维素;C 氕与氘;D 甲烷与戊烷; E 葡萄糖与果糖
F![]() 与
与 G
G  与
与
其中互为同位素 _____;(填编号.下同),互为同系物的是____,互为同分异构体的是______,是同一种物质的是________.
(2)化合物A的结构简式为: ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_____;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为_____。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_____;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为_____。
(3)篮烷分子的键线式如图所示,试回答:

写出篮烷分子的化学式________;篮烷分子的一氯取代物的种数为______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的基本化工原料,可制备乙酸乙酯,其转化关系如图.

已知:H2C=CH﹣OH不稳定
I ①的反应类型是___.请写出乙烯官能团名称_____, 由A生成B的化学方程式_____.
II 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。

已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;
②有关有机物的沸点见下表:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用为_______;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式__________
(2)球形干燥管C的作用是______若反应前D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出________;再加入(此空从下列选项中选择)________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A 五氧化二磷 B 碱石灰
C 无水硫酸钠 D 生石灰
(4)从绿色化学的角度分析,使用浓硫酸制乙酸乙酯不足之处主要有________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是

A. t1℃时,30gB物质溶解在50g水中形成80g溶液
B. t2℃时,不能配成溶质质量分数相同的三种物质的饱和溶液
C. 当A中混有少量C时,可采用冷却热饱和溶液法提纯A
D. A、C两种物质的饱和溶液从t2℃降到t1℃时,溶液的溶质质量分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,还含有少量SiO2。现以卤块为原料按如图所示流程进行生产,用于制备金属镁。

请回答下列问题:
(1)步骤①中,为了加快酸溶速率,除了适当增加稀盐酸的浓度外,还可以采取的措施是____________(任写一条)。
(2)步骤②得到的X是___(填化学式),能够分离得到沉淀的方法是_____
(3)写出步骤④的化学方程式:_______
(4)步骤①中溶解卤块的盐酸如果过量太多造成的影响是____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为短周期元素,它们在元素周期表中的相对位置如图所示,其中B的单质在空气中含量约占80%。
A | B | C | |||
D |
(1)写出下列元素的名称:C____,D___。
(2)画出B的原子结构示意图____。C在元素周期表中的位置是____。
(3)B、C两种元素最简单氢化物的稳定性由强到弱的顺序是_____。写出A的最简单氢化物的电子式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小王同学准备用CuSO4·5H2O配制500mL 1 mol/L的溶液。
(1)小王同学选用的玻璃仪器有:烧杯,玻璃棒,__________;________。
(2)玻璃棒在该实验中有重要的用途,分别是__________和 _________;
(3)小王同学通过计算,用托盘天平称取________gCuSO4·5H2O。
(4)物质的量浓度误差(填偏高、偏低、无影响)
①若容量瓶中洗净后未干燥,残留少量水,则所配制的溶液浓度将_________;
②定容时,若眼睛俯视,则所配制的溶液浓度将___________;
③摇匀后以免低于刻度线,再加入少量水________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com