
苯分子实际上不是碳破单键和碳碳双健的交替结构,下列不可以作为证据的事实有( )
①苯的间位二元取代物只有一种
②苯的邻位二元取代物只有一种
③苯不能使酸性高锰酸钾溶液褪色
④苯能在一定条件下与氢气反应生成环己烷
⑤苯在FeBr3存在的条件下同液溴发生反应
A. ①④ B. ③④ C. ②③ D. ①⑤
科目:高中化学 来源:2016-2017学年河南省高二上开学测化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. 放热反应在常温下一定是很容易发生
放热反应在常温下一定是很容易发生
B.需要加热才能发生的反应一定是吸热反应
C.在稀溶液中,1 mol酸与1mol碱发生中和反应时所释放的热量叫中和热
D.一个反应是放热还是吸热,主要取决于反应物总能量与生成物总能量的相对大小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上开学测化学试卷(解析版) 题型:填空题
在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g) + H2O(g)  CO2(g) + H2(g)△H<0。CO和H2O(g)浓度变化如右图
CO2(g) + H2(g)△H<0。CO和H2O(g)浓度变化如右图
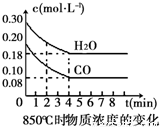
(1)0~4min的平均反应速率v(CO)=___________mol•L-1•min-1.
(2)该条件下,此反应的平衡常数K=___________(写表达式).
(3)该反应平衡时CO的转化率为________________。
(4)能判断该反应达到化学平衡状态的依据是______________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
(5)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表.

① c1数值___________0.08mol•L-1(填大于、小于或等于).
②反应在4min~5min间,平衡向逆方向移动,可能的原因是________________,表中5min~6min之间数值发生变化,可能的原因是_______________。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上开学测化学试卷(解析版) 题型:选择题
下列物质中既含有离子键又含有共价键的是( )
A.HCl B.KOH C.I2 D.Na2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上开学测化学试卷(解析版) 题型:填空题
恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g) + 3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=______________.
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量______________.
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=_____________.
(4)达到平衡时,N2和H2的转化率之比,α(N2):α(H2)=______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上开学测化学试卷(解析版) 题型:选择题
新型NaBH4/H2O2燃料电他(DBFC)的结构如下图.该电池总反应方程式:NaBH4+4H2O2=NaBO2+6H2O,有关的说法正确是( )

A.电池正极区的电极反应为:BH4-+8OH--8e-=BO2-+6H2O
B.电极B为负极,纳米MnO2层的作用是提离原电池的工作效率
C.放电过程中,Na+从正极区向负极区迁移
D.在电池反应中,每消耗1L 6mol/L H2O2溶液,理论上流过电路中的电子为12NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上开学测化学试卷(解析版) 题型:选择题
某元素X的最高价含氧酸的化学式为HnXO2n-2,则在其气态氢化物中,X元素的化合价为( )
A. 3n-6 B. 5n-12 C. 3n-12 D. n-10
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三第一次摸底化学试卷(解析版) 题型:实验题
过氧化钙较稳定,不溶于乙醇,微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。

回答下列问题:
(1)大理石经过溶解、沉淀、过滤、在沉淀、再过滤,得到CaCO3,其目的是 ;过滤需要用到的玻璃仪器主要有漏斗、烧杯和 。
(2)反应①的具体操作作为逐滴加入稀盐酸,至溶液中尚存有少量固体。将溶液煮沸,趁热过滤。将溶液煮沸的作用是 。
(3)反应②的化学方程式为 ,该反应需要在冰浴下进行,原因是 。
(4)白色晶体水洗时,判断是否洗净的方法是 ;使用乙醉洗涤的目的是 。
(5)制备过氧化钙的另一种方法是:将石灰石锻烧后.直接加人双氧水反应,过滤后可得到过氧化钙产品。该法的优点是工艺简单、操作简单.所得产品的缺点是 。
(6)CaO2·8H2O加热脱水的过程中,需不断通入氧气.目的是抑制过氧化钙分解。若通入的氧气中混有二氧化碳,其后果是 ;已知CaO2在350℃迅速分解生成CaO和O2。下图是实验室测定产品中CaO2含量的装置(夹持装置省略)。

若所取产品质量为ag,测得生成气体的体积为VmL(已换算成标准状况),则产品中CaO2的质量分数为 (用含a、V的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期摸底化学试卷(解析版) 题型:选择题
下列叙述正确的有几项
①氯化钠溶液能导电,所以氯化钠溶液是电解质
②BaSO 4 投入水中,导电性较弱,故它是弱电解质
③氯化氢水溶液能导电,所以氯化氢是电解质
④三氧化硫溶于水能导电,所以三氧化硫是电解质
⑤铜能导电,所以是电解质
⑥CaCO 3 投入水溶液几乎不能导电,但CaCO 3 是强电解质
⑦氯气溶于水能导电所以氯气为电解质
A.1 B.2 C .3 D. 4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com