
【题目】共价键不可能存在于
A.金属单质B.非金属单质C.离子化合物D.共价化合物
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A | 在恒容密闭容器中,可逆反应C(s)+H2O(g) | 正反应选率将逐渐增大 |
B | 比较硅和碳的还原性 | 利用反应:SiO2+2C |
C. | 氯气具有漂白性 | 氯气通入滴有酚酞的NaOH溶液,溶液褪色 |
D | 证明氯气与水反应生成酸性物质,且该反应为可逆反应 | 少量氯气通入大量水中,测定溶液pH<7且显浅黄绿色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的
B.乙醇、乙烯、乙醛都能使酸性高锰酸钾溶液褪色
C.豆科作物根瘤菌将含氮化合物转化为蛋白质是氮的固定
D.核电站泄漏的放射性碘﹣131( ![]() I)、铯﹣137(
I)、铯﹣137( ![]() Cs)互称同位素,可使蛋白质变性
Cs)互称同位素,可使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
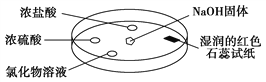
选项 | 实验现象 | 解 释 |
A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应产生了微小的NH4Cl晶体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
D | 湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁[Fe2(OH)n(SO4)3﹣n/2]m是一种新型高效的水处理混凝剂,某课题小组设计如下方案制备聚合硫酸铁,其简单工艺流程如图1:
为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2 , 调节pH<3,加热煮沸;加入过量KI充分反应后,再用0.1 000molL﹣1 Na2S2O3标准溶液滴定至终点,消耗标准溶液VXmL.已知:I2+2S2O32﹣═I﹣+S4O62﹣ . .
(1)实验过程中加热煮沸的目的是 .
(2)在测定过程中加入足量H2O2发生反应离子方程式: .
(3)滴定过程中选择装标准溶液仪器(如图2)是否合理(填“是”或“否”)
(4)写出滴定选用的指示剂 , 滴定终点观察到的现象 .
(5)根据图1消耗的Na2S2O3标准溶液体积,计算出溶液Ⅰ中铁元素的总含量为gL﹣1 . 若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会(填“偏高”“偏低”或“不变”).
(6)上述流程中溶液Ⅰ中铁元素存在不同的离子,根据题意完成下面假设并设计实验方案证明假设假设1:溶液Ⅰ中只存在Fe2+ 假设2:溶液Ⅰ中只存在Fe3+ 假设3: .
根据提供试剂和实验用品验证假设3成立
限选实验试剂:1.0molL﹣1 NaOH溶液、8.0molL﹣1 NaOH溶液、0.01molL﹣1KMnO4、淀粉﹣KI溶液、3moLL﹣1H2SO4、紫色石蕊试液、0.1molL﹣1 K3[Fe(CN)6]溶液、试管、胶头滴管
实验步骤 | 预期现象和结论 |
步骤1:取少量溶液Ⅰ于试管A、B中 | |
步骤2: | |
步骤3: |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列叙述正确的是(相对原子质量O﹣16 Na﹣23)( )
A.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH﹣数目为0.2NA
B.100 mL 1 molL﹣1的H2SO4溶液中含有0.1NA个H+
C.将4 g NaOH溶于100 g蒸馏水中,所得溶液物质的量浓度是0.1 molL﹣1
D.20g重水(D2O)所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧可用于净化空气、饮用水的消毒、处理工业废物和作氧化剂.
(1)臭氧几乎可与除铂、金、铱、氟以外的所有单质反应.如:6Ag(s)+O3(g)═3Ag2O(s)△H=﹣235.8kJ/mol.
已知2Ag2O(s)═4Ag(s)+O2(g)△H=+62.2kJ/mol,
则常温下反应:2O3(g)═3O2(g)的△H= .
(2)科学家首先使用在酸性条件下电解水的方法制得臭氧.臭氧在阳极周围的水中产生,电极反应式为3H2O﹣6e﹣=O3↑+6H+ , 阴极附近溶解在水中的氧气生成过氧化氢,其电极反应式为 .
(3)O3在碱性条件下可将Na2SO4氧化成Na2S2O8并生成氧气.写出该反应的化学方程式:
(4)所得的Na2S2O8溶液可降解有机污染物4﹣CP.原因是Na2S2O8溶液在一定条件下可产生强氧化性自由基(SO4﹣).通过测定4﹣CP降解率可判断Na2S2O8溶液产生SO4﹣的量.某研究小组设计实验探究了溶液酸碱性、Fe2+的浓度对产生SO4﹣的影响.①溶液酸碱性的影响:其他条件相同,将4﹣CP加入到不同pH的Na2S2O8溶液中,结果如图a所示.由此可知:溶液酸性增强,(填“有利于”或“不利于”)Na2S2O8产生SO4﹣ . 
②Fe2+浓度的影响:相同条件下,将不同浓度的FeSO4溶液分别加入c(4﹣CP)=1.56×10﹣4molL﹣1、c(Na2S2O8)=3.12×10﹣3 molL﹣1的混合溶液中.反应240min后测得实验结果如图b所示.已知 S2O82﹣+Fe2+═SO4﹣+SO42﹣+Fe3+ . 则由图示可知下列说法正确的是:(填序号)
A.反应开始一段时间内4﹣CP降解率随Fe2+浓度的增大而增大,原因是Fe2+能使Na2S2O8产生更多的SO4ˉ.
B.Fe2+是4﹣CP降解反应的催化剂
C.当c(Fe2+)过大时,4﹣CP降解率反而下降,原因可能是Fe2+会与SO4﹣发生反应,消耗部分SO4﹣.
D.4﹣CP降解率反而下降,原因可能是生成的Fe3+水解使溶液的酸性增强,不利于4﹣CP的降解.
③当c(Fe2+)=3.2×10ˉ3molL﹣1时,4﹣CP降解的平均反应速率的计算表达式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
阳离子 | Na+、Al3+、Ba2+、NH4+ |
阴离子 | Cl﹣、OH﹣、CO32﹣、SO42﹣ |
分别取四种物质进行实验,实验结果如下
①B溶液分别与C,D混合,均有白色沉淀生成;
②将A溶液逐滴滴入C溶液中,有沉淀生成,继续滴加A溶液时,沉淀减少直至完全消失;
③A与D两种固体混合加热有气体生成,该气体能使湿润的红色石蕊试液变蓝;
④用石墨电极电解B溶液,在阳极上产生一种有刺激性气味的气体.
(1)A所含的阴离子的电子式是 , B所含的阳离子是 .
(2)C的化学式是 , D的化学式是 .
(3)写出②中沉淀溶解的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com