
【题目】
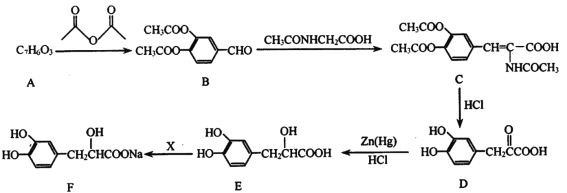
丹参素是中药丹参的水溶性成分,结构为 F ,具有扩张血管、增加冠脉血流量等作用,某一种合成路线如下图所示:
已知:![]()
![]()
(1)丹参素的分子式为____________; D →E 的反应类型是_______________。
(2)试剂X是____________(写化学式);C 中含氧官能团名称为_____________。
(3) A→B 的反应方程式为________________。
(4)G与 E互为同分异构体,请写出满足下列条件的任意两种G的结构简式______________。
①lmolG 能与4molNaOH发生反应;
②能够发生水解反应;
③核磁共振氢谱显示5个吸收峰,且峰面积之比为 1 : 2 : 2 : 2 : 3 。
(5)参考上述流程信息,设计以![]() 、CH3CHO为原制取
、CH3CHO为原制取![]() 的合成路线(其它无机试剂任选)。________________
的合成路线(其它无机试剂任选)。________________
【答案】C9H9O5Na 还原反应 NaHCO3 酯基、羧基、肽键 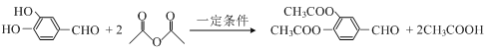 或
或
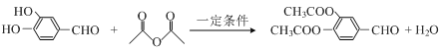 以下任选两种
以下任选两种


【解析】
根据有机物组成、结构的变化,判断反应类型,书写反应方程式;根据概念和题目要求写同分异构体;紧扣信息和已学化学反应设计合成路线。
(1)据丹参素的结构简式(F)得分子式C9H9O5Na;比较结构知,D →E 即![]() 变成
变成![]() ,是有机物加氢的还原反应。
,是有机物加氢的还原反应。
(2)E →F只有-COOH变成-COONa,醇羟基、酚羟基都不变,则试剂X是NaHCO3,不可用Na2CO3、NaOH。C 中含氧官能团有酯基、羧基、肽键。
(3)根据“已知”中的前一个反应,A的结构简式为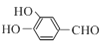 ,A→B 的化学方程式为:
,A→B 的化学方程式为: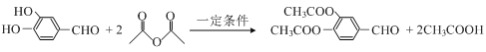
(或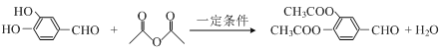 )。
)。
(4)G与 E互为同分异构体,分子式都是C9H10O5。G能发生水解反应必有酯基,E除苯外只有一个双键,即G只能有一个酯基。要lmolG 与4molNaOH反应,则为一个醇酯基和三个酚羟基,或一个酚酯基和两个酚羟基。要G中5种氢原子,且数目比为 1 : 2 : 2 : 2 : 3,G分子有较好的对称性,且有一个-CH3。由此写出两种符合要求的结构简式。
(5)应用“已知”中的后一个反应,可将醛基的αH与另一分子的醛基“拼接”,故应将![]() 氧化为
氧化为![]() 。因酚羟基有较强的还原性,氧化前须用NaOH溶液或(CH3CO)2O保护酚羟基。主体反应完成后,再将酚羟基恢复。可能的合成路线:
。因酚羟基有较强的还原性,氧化前须用NaOH溶液或(CH3CO)2O保护酚羟基。主体反应完成后,再将酚羟基恢复。可能的合成路线:



科目:高中化学 来源: 题型:
【题目】以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
选项 | 氧化物 | 环境问题 | 主要来源 |
A | CO2 | 破坏臭氧层 | 化石燃料的燃烧 |
B | SO2 | 温室效应 | 汽车尾气的排放 |
C | NO2 | 光化学烟雾 | 工厂废气的排放 |
D | CO | 酸雨 | 汽车尾气和化石燃料的不完全燃烧 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃结构简式为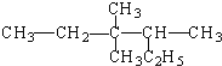 ,其命名正确的是
,其命名正确的是
A. 2-乙基-3,3-二甲基戊烷 B. 3,3-二甲基-4-乙基戊烷
C. 3,3,4-三甲基己烷 D. 3,4,4-三甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为纳米二氧化锰燃料电池,其电解质溶液呈酸性,已知(CH2O)n中碳的化合价为0价,有关该电池的说法正确的是

A. 放电过程中左侧溶液的pH降低
B. 当产生22gCO2时,理论上迁移质子的物质的量为4mol
C. 产生22gCO2时,膜左侧溶液的质量变化为:89g
D. 电子在外电路中流动方向为从a到b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核内中子数为N的R2+,质量数为A,则ng它的同价态氧化物中所含电子物质的量为( )
A.![]() (A+N-10)molB.
(A+N-10)molB.![]() (A-N+6)mol
(A-N+6)mol
C.(A-N+2)molD.![]() (A-N+8)mol
(A-N+8)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式及其叙述正确的是( )
A. 氢气的燃烧热为285.5 kJ·mol·-1,则水分解的热化学方程式为:2H2O(l)=2H2+O2(g)ΔH=+285.5 kJ·mol-1
B. 已知2C(石墨,s)+O2(g)=2CO(g)ΔH=-221 kJ·mol-1,则石墨的燃烧热为110.5 kJ·mol-1
C. 已知N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应后最多可放出92.4 kJ的热量
2NH3(g)ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应后最多可放出92.4 kJ的热量
D. 已知乙醇和乙烯的燃烧热分别为1 366.8 kJ·mol-1和1 411.0 kJ·mol-1,则乙烯水化制乙醇的热化学方程式为:C2H4(g)+H2O(l)=C2H5OH(l) ΔH=-44.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过量铝粉分别与下列4种等体积的溶液充分反应,放出氢气最多的是( )
A.3mol·L-1H2SO4溶液B.18mol·L-1H2SO4溶液
C.1.5 mol·L-1KOH溶液D.3mol·L-1HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是很好的净水剂,高铁酸钡( BaFeO4)是高能电池阳极的优良材料。已知:K2FeO4为紫色固体,微溶于KOH溶液,在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定;在碱性溶液中,NaCl、NaNO3、K2FeO4的溶解性都小于Na2FeO4;BaFeO4难溶于水和碱性溶液。某化学兴趣小组欲制取“84”消毒液,进而制取少量K2FeO4和 BaFeO4。请回答下列问题:
(实验一)选择合适的仪器和试剂制取氯气,进而制备高浓度的“84”消毒液。
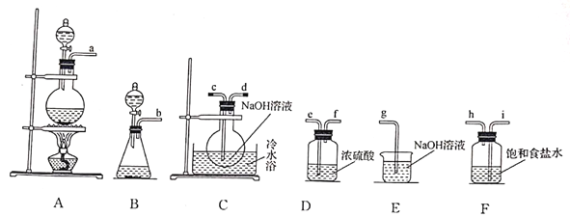
(1)选择合适的仪器,导管接口正确的连接顺序为___________;所选装置(A或B)中发生反应的离子方程式为______________________。
(实验二)用“84”消毒液制取K2FcO4
实验步骤:①用如图所示装置(夹持仪器略去)使反应物充分反应;②用砂芯漏斗对烧杯中的溶液进行抽滤,向滤液中慢慢加入KOH溶液;③再用砂芯漏斗对步骤②的最后反应混合物进行抽滤,并用苯、乙醚洗涤沉淀,真空干燥后得K2FeO4。

(2)写出步骤①中物质在20℃冷水浴中发生反应的化学方程式:______________________。
(3)步骤②中能够发生反应的原因是______________________,步骤③中不用水,而用苯、乙醚洗涤沉淀的目的是_________________________________。
(实验三)将上述产品配成K2FeO4碱性溶液,再慢慢加入Ba(OH)2溶液,抽滤得 BaFeO4。
(4)若投入ag硝酸铁晶体,得到bg高铁酸钡,则高铁酸钡的产率是___________。[已知Fe(NO3)3·9H2O的摩尔质量为404g·mol-1, BaFeO4的摩尔质量为257g·mol-1]
(实验四)利用如图所示电解装置也可以制得 BaFeO4。

(5)在___________(填“阳极区”或“阴极区”)可得到高铁酸钡,阳极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。一种回收废旧磷酸亚铁锂电池正极片(主要成分LiFePO4、炭黑和铝箔)中金属的流程如下:
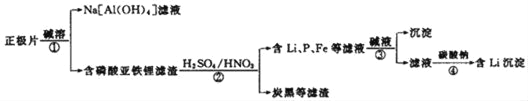
(1)步骤①中“碱溶”反应的化学方程式为_____。
(2)步骤②中反应的离子方程式为_____。若用H2O2代替HNO3,其优点是_____。
(3)步骤③沉淀的主要成分是_____。
(4)步骤④中生成含Li沉淀_____(填“能”或“不能”)用硫酸钠代替碳酸钠,原因是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com