
某芳香族化合物H(C11H12O4)是有机合成工业的一种重要的中间产物,其合成路线如下。已知2molC分子可缩合生成1mol六元环化合物分子。F常温下是气体,水溶液具有很好的防腐杀菌效果,且能与新制氢氧化铜反应。请回答下列问题:

49.F的电子式为 , A的结构简式
B转化为C的条件是
A.水解、酸化、氧化、还原 B.氧化、水解、酸化、还原
C.水解、酸化、还原、氧化 D.氧化、酸化、水解、还原
50.以C为原料可合成可降解塑料,试写出其化学方程式
51.H与氢氧化钠溶液反应的化学方程式
52.H的同分异构体有多种,请写出符合下列条件的同分异构体的结构简式
。(写两种即可)
①苯环上只有两个取代基,苯环上的一氯取代物只有两种
②1mol的H与足量的NaHCO3溶液反应,生成2molCO2
49.  (2分),CH3CH=CH2(2分) A (2分)
(2分),CH3CH=CH2(2分) A (2分)
50. 
51. 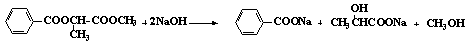
52.(任写1种2分)  、
、 、
、
 、
、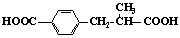
 、
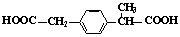
、
【解析】
试题分析:49.F常温下是气体,水溶液具有很好的防腐杀菌效果,且能与新制氢氧化铜反应,说明F分子中含有醛基,常温下是气体的醛是甲醛,所以F的结构简式为HCHO;与氢气发生加成反应生成甲醇,所以G是甲醇;C、E、G三种物质反应生成的H中含有11个C原子,所以A中含有3个C原子,且A能与溴的四氯化碳溶液反应,所以A中含有不饱和键, A为丙烯,结构简式为CH2=CHCH3。2molC分子可缩合生成1mol六元环化合物分子,则C是2-羟基丙酸, F的电子式为 ;B是丙烯与溴的加成产物1,2-二溴丙烷,生成2-羟基丙酸,需要先在氢氧化钠溶液中发生水解反应生成1,2-丙二醇,然后酸化溶液后向其中加入氧化剂氧化羟基,得2-羰基丙酸,再加入还原剂将羰基还原为羟基即可得到2-羟基丙酸,所以答案选A。
;B是丙烯与溴的加成产物1,2-二溴丙烷,生成2-羟基丙酸,需要先在氢氧化钠溶液中发生水解反应生成1,2-丙二醇,然后酸化溶液后向其中加入氧化剂氧化羟基,得2-羰基丙酸,再加入还原剂将羰基还原为羟基即可得到2-羟基丙酸,所以答案选A。
50. 以2-羟基丙酸为原料,生产降解塑料,则应发生缩聚反应,化学方程式为
 。
。
51.根据流程图可知,D是甲苯,E是苯甲酸,由C、G、E三种物质的结构简式可知,三者发生酯化反应生成H,因为C中存在羟基与羧基,可与苯甲酸、甲醇分别发生酯化反应,所以H的结构简式为 ,则H在碱性条件下发生水解反应,生成苯甲酸钠、甲醇、与2-羟基丙酸钠,化学方程式为
,则H在碱性条件下发生水解反应,生成苯甲酸钠、甲醇、与2-羟基丙酸钠,化学方程式为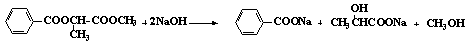 。
。
52.H的结构简式为 ,同分异构体中,苯环上只有两个取代基,苯环上的一氯取代物只有两种,则者两种取代基位于对位;1mol的H与足量的NaHCO3溶液反应,生成2molCO2
,同分异构体中,苯环上只有两个取代基,苯环上的一氯取代物只有两种,则者两种取代基位于对位;1mol的H与足量的NaHCO3溶液反应,生成2molCO2
,说明H的同分异构体中存在2个羧基,根据 H的侧链取代基C原子的数目,两个取代基中C原子数目之和是5,按照“此增彼减”的原则,判断取代基的种数加快,所以符合题意的H的同分异构体有6种,分别是 、
、 、
、 、
、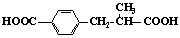
 、
、 。
。
考点:考查有机物的推断与合成,化学方程式的书写,同分异构体的判断与书写


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年四川省达州市普高高三上学期第一次诊断理综化学试卷(解析版) 题型:填空题
(16分)钛合金是航天航空工业的重要原料。由钛铁矿(主要成分是TiO2和Fe的氧化物)
制备Ti和绿矾(FeSO4·7H2O)等产品的一种工艺流程示意如下

已知:①TiO2+易水解,只能存在于强酸性溶液中 ②TiCl4的熔点-25℃,沸点136.4℃;SiCl4的熔点-68.8℃,沸点57.6℃ 回答下列问题:
(1)TiCl4的晶体类型是 晶体。
(2)TiO2的天然晶体中,最稳定的一种晶体结构如图,其中黑球表示 原子。

(3)钛铁矿酸浸时,主要成分TiO2反应的离子方程式为 。
(4)操作Ⅱ包含的具体操作方法有 。
(5)废液中溶质的主要成分是 (填化学式)。
(6)沸腾氧化炉中发生反应的化学方程式为 ,
制得的TiCl4液体中常含有少量SiCl4杂质,可采用 方法除去。
(7)若经事先处理后的钛铁矿只含有TiO2和Fe3O4两种氧化物,现有312kg经处理后的钛铁矿,经上述流程后(省去操作Ⅰ)制得了48kg纯净的金属钛。已知在上述流程的强酸性溶液中加过量铁粉时测得转移的电子的物质的量为2a×103mol,则理论上可制得 kgFeSO4·7H2O(假设上述各步反应均完全且各步没有损耗)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:填空题
(本题共12分)已知: (X为卤原子,M为烃基或含酯基的取代基等)
(X为卤原子,M为烃基或含酯基的取代基等)
由有机物A合成G(香豆素)的步骤如下:

回答下列问题:
47.写出反应C+D→E的反应类型 。
48.A中官能团名称为 ;写出反应条件:E→F 。
49.写出结构简式:B ,D 。
50.F有多种同分异构体,写出同时满足下列条件的任意两种同分异构体的结构简式: 。
① 分子中除苯环外,无其它环状结构;
② 分子中有四种不同化学环境的氢原子;
③ 能发生水解反应,不能与金属钠反应;
④ 能与新制Cu(OH)2按物质的量之比1:2反应。
51.二氢香豆素( )常用作香豆素的替代品。鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品。鉴别二氢香豆素和它的一种同分异构体( )需要用到的试剂有:NaOH溶液、 。
)需要用到的试剂有:NaOH溶液、 。
52.已知: (R,R′为烃基)。试写出以苯和丙烯(
(R,R′为烃基)。试写出以苯和丙烯( =CH—CH3)为原料,合成
=CH—CH3)为原料,合成 的路线流程图(无机试剂任选)。合成路线流程图示例如下:
的路线流程图(无机试剂任选)。合成路线流程图示例如下:






查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
除杂和配制试剂是中学化学中常见的实验。对实验方法描述正确的是
A.用蒸发结晶法除去KNO3中少量的NaCl
B.用加入NaOH(aq)并蒸馏的方法除去乙醛中少量的乙酸
C.准确称取14.800g Ca(OH)2,配制100mL 2.0 mol/L的Ca(OH)2溶液
D.在2mL10%的CuSO4(aq)中滴入3滴 2%的NaOH(aq),配制检验醛基的试剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
物质的用途错误的是
A.草酸可用于提炼稀有金属 B.苯酚可用于制造酚醛树脂
C.浓硫酸可用于实验室制取HCl(g) D.氯化铵溶液可用于除去金属表面油污
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:填空题
探究外界条件对化学反应速率的影响常用到该反应
已知:Na2S2O3+H2SO4→Na2SO4+S↓+SO2+H2O
针对上述反应涉及到的元素或物质及性质回答有关问题:
23.硫元素的化合价由高到低顺序为:______________________________
涉及元素的简单离子半径由小到大顺序为:______________________________;
24.氧原子的最外层电子排布轨道表示式:______________________________;
列举2个能说明氧、硫两种元素非金属性强弱事实:______________________________;
25.预测镁在二氧化硫中燃烧的现象:________________________________________
产物除氧化镁、硫磺外还可能有 生成。
26.下面是某同学是根据该反应实验数据绘制的图表

该同学得出的结论是:
_________________________________________________________________________________。
27.将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀,用电离平衡原理解释上述现象。
_________________________________________________________________________________。
若继续通入另两种气体如Cl2 和H2S也会产生沉淀,请用化学方程式表示生成沉淀的原理。
_________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:选择题
羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得。

(羟基扁桃酸)
下列有关说法正确的是
A.苯酚和羟基扁桃酸互为同系物
B.标准状况下,22.4L羟基扁桃酸中共用电子对的数目为24 NA
C.乙醛酸只存在一种不同环境的氢原子
D.羟基扁桃酸分子中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市虹口区高三上学期期末考试化学试卷(解析版) 题型:填空题
(本题共12分)
M(结构简式: )不溶于水,是一种昂贵的食用香料,也是重要的医药中间体。M的一条合成路线如下(部分反应试剂和条件略去),且D与M互为同分异构体。
)不溶于水,是一种昂贵的食用香料,也是重要的医药中间体。M的一条合成路线如下(部分反应试剂和条件略去),且D与M互为同分异构体。

已知︰
完成下列填空:
50.写出反应类型。 反应①_____________ 反应⑦_____________
51.写出结构简式。 A_________________ D__________________
52.写出检验E已完全转化为M的方法_______________________________。
53.写出一种满足下列条件C的同分异构体的结构简式(不考虑立体异构)___________。
i.能发生银镜反应
ii.无环状结构
iii.分子中有2种化学环境不同的氢原子
54.完成以C3H6为有机原料制备丙酸(CH3CH2COOH)(其他无机原料任选)的合成路线。
(合成路线的常用表示方法为: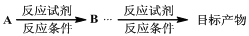 )
)
55.反应③的目的是_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市长宁区高三上学期教学质量检测化学试卷(解析版) 题型:选择题
向饱和澄清石灰水中加入少量CaC2,充分反应后立即测定所得溶液中离子浓度,下列预测正确的是
A.c(Ca2+)、c(OH―)一定增大 B.c(Ca2+)、c(OH―)一定保持不变
C.c(Ca2+)、c(OH―)均可能减小 D.c(OH―)增大、c(H+)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com