
| A. | 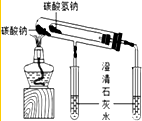 比较碳酸钠与碳酸氢钠的热稳定性 | B. |  称取NaOH | ||
| C. | 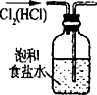 除去Cl2中HCl | D. | 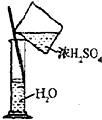 稀释浓H2SO4 |
分析 A.碳酸氢钠受热温度低分解,大试管温度高,碳酸钠不分解;
B.NaOH易潮解,具有腐蚀性,应在小烧杯中称量;
C.除杂时导管应长进短出;
D.不能在量筒中稀释浓硫酸.
解答 解:A.碳酸氢钠受热温度低分解,大试管温度高,碳酸钠不分解,则图中装置可比较热稳定性,故A正确;
B.NaOH易潮解,具有腐蚀性,应在小烧杯中称量,图中操作不合理,故B错误;
C.除杂时导管应长进短出,图中导管的进气方向不合理,故C错误;
D.不能在量筒中稀释浓硫酸,应在烧杯中稀释,量筒只能量取液体的体积,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、实验装置的作用、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验操作及实验评价性分析,题目难度不大.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 气体发生装置 | 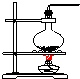 a |  b | 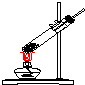 c |
| 气体收集装置 | 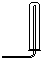 ① |  ② | 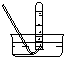 ③ |

查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
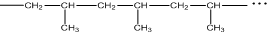 合成该高分子化合物的单体是( )
合成该高分子化合物的单体是( )| A. | CH2=CH2 | B. | CH2=CH-CH3 | C. | CH3CH2CH3 | D. | CH3CH(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
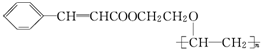
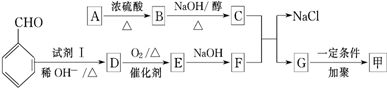
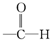 +
+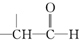 $→_{△}^{稀OH-}$
$→_{△}^{稀OH-}$ +H2O
+H2O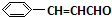 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2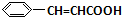 +H2O;③C与F的反应:
+H2O;③C与F的反应: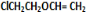 +
+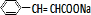 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$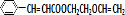 +NaCl.
+NaCl.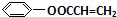 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com