
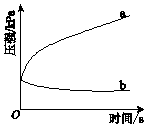
 生铁在pH=2和pH=4的盐酸中发生腐蚀.在密闭容器中,用压强传感器记录该过程的压强变化,如图所示.下列说法中,不正确的是( )
生铁在pH=2和pH=4的盐酸中发生腐蚀.在密闭容器中,用压强传感器记录该过程的压强变化,如图所示.下列说法中,不正确的是( )| A. | 两容器中负极反应均为Fe-2e-═Fe2+ | |
| B. | 曲线a记录的是pH=2的盐酸中压强的变化 | |
| C. | 曲线b记录的容器中正极反应是O2+4e-+2H2O═4OH- | |
| D. | 在弱酸性溶液中,生铁能发生吸氧腐蚀 |
分析 据压强与时间关系图知,曲线a的压强随着反应的进行而逐渐增大,说明发生析氢腐蚀,对应的是酸性较强的pH=2的盐酸溶液;曲线b的压强随着反应的进行而逐渐减小,说明发生吸氧腐蚀,对应的应是酸性较弱的pH=4的盐酸溶液,根据原电池原理来分析解答.
解答 解:A.两个溶液中都发生电化学腐蚀,铁均作负极,电极反应式为Fe-2e-=Fe2+,故A正确;
B.曲线a的压强随着反应的进行而逐渐增大,说明发生析氢腐蚀,发生析氢腐蚀的条件是酸性较强,则该容器中的盐酸pH=2,故B正确;
C.曲线b的压强随着反应的进行而逐渐减小,说明发生吸氧腐蚀,对应的应是酸性较弱的pH=4的盐酸溶液,电解质溶液呈酸性,正极反应为O2+4e-+4H+═2H2O,故C错误;
D.曲线b的压强随着反应的进行而逐渐减小,说明发生吸氧腐蚀,对应的应是酸性较弱的pH=4的盐酸溶液,所以在酸性溶液中生铁可能发生吸氧腐蚀,故D正确;
故选C.
点评 本题考查了析氢腐蚀和吸氧腐蚀,根据压强与时间的关系分析吸氧腐蚀和析氢腐蚀、电极反应等知识点,注意弱酸性条件下生铁能发生吸氧腐蚀,难度中等.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
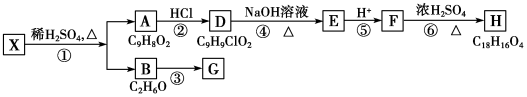
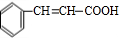 ,检验A中非含氧官能团所用的试剂为溴水或溴的四氯化碳溶液.
,检验A中非含氧官能团所用的试剂为溴水或溴的四氯化碳溶液.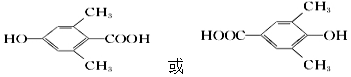 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定序号 | 待测液体积(ml) | 所消耗盐酸标准液的体积(ml) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
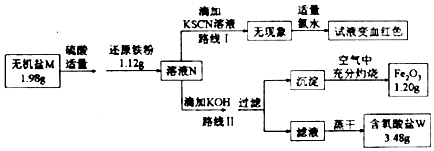
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  | 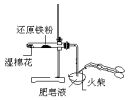 | 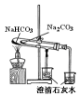 |
| 验证:溶解性AgCl>AgBr>Ag2S | 验证:非金属性Cl>C>Si | 验证:铁粉与水蒸气反应产生的氢气 | 验证:热稳定性 Na2CO3>NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 分别向2mL0.1mol/LNaHCO3,和2mL0.1mol/LNa2CO3溶液中滴加2mL 0.2mol/L的盐酸 | 盛有NaHCO3溶液试管产生气泡速度快 | 结合H+能力CO32->HCO3- |
| B | 将石蜡油(烷烃)蒸汽通过灼热的碎瓷片,并将产生的气体通人溴的四氯化碳溶液 | 溴的四氯化碳溶液褪色 | 生成气体中含有不饱和烃 |
| C | 向KI溶液中加入淀粉,然后滴入稀硫酸数滴 | 开始无明显现象,片刻溶液变蓝 | 氧化性:H2SO4>I2 |
| D | 向某溶液中加入盐酸 | 产生刺激性气味的气体和黄色沉淀 | 溶液中一定存在S2O32- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
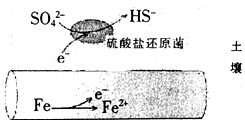 深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图示,下列与此原理有关说法错误的是( )
深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图示,下列与此原理有关说法错误的是( )| A. | 正极反应为:SO42-+5H2O+8e-=HS-+9OH- | |
| B. | 输送暖气的管道不易发生此类腐蚀 | |
| C. | 这种情况下,Fe腐蚀的最终产物为Fe2O3•xH2O | |
| D. | 管道上刷富锌油漆可以延缓管道的腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 将C2H4和SO2的混合气体通入足量酸性KmnO4试液中 | 得到纯净的C2H4 |
| B | 向5mL 0.1mol•L-1AgNO3溶液中加1mL0.1mol•L-1NH3•H2O | 制备银氨溶液 |
| C | 向含少量FeBr2的FeCl2溶液中滴入适量新制氯水,并加入CCl4萃取分液 | 制备纯净的FeCl2溶液 |
| D | 向NaCl饱和溶液中先通入NH3至饱和,再通入足量CO2,过滤并洗涤 | 制备NaHCO3固体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com