


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列实验事实所引出的相应结论正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、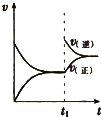 表示:反应I2(g)+H2(g)?2HI(g)△H<0的v-t关系,其中t1时刻改变的条件为升高温度 | B、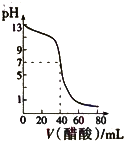 表示:25℃时,用醋酸溶液滴定40.00mL 0.1000mol?L-1 NaOH溶液的滴定曲线,其中c(CH3COOH)=0.1000mol?L-1 | C、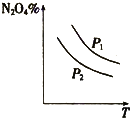 表示:反应2NO2(g)?N2O4(g)的平衡体系中,N2O4的百分含量与温度(T)、压强(P)的变化关系,其中△H<0、P1<P2 | D、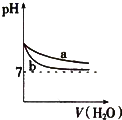 表示:25℃时,分别稀释等体积,等pH的NaOH溶液与氨水时的pH变化,其中曲线a对应氨水 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省嘉峪关一中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com