
【题目】由A、B、C、D四种金属按下表中装置图进行实验.

根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_____________________________________.
(2)装置乙中正极的电极反应式是____________________________________..
(3)四种金属活泼性由强到弱的顺序是__________________________________.
(4)A、C形成合金,露置在潮湿空气中,_______先被腐蚀。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
A.K+、Na+、HCO3-、NO3-
B.Na+、SO42-、Cl-、ClO-
C.H+、Mg2+、SO42-、NO3-
D.Ag+、K+、NO3-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 为提纯下列物质,所选除杂试剂和分离的主要操作方法都合理的是( )
选项 | 被提纯的物质(杂质) | 除杂试剂 | 主要操作方法 |
A | NaHCO3溶液(Na2CO3) | 澄清石灰水 | 过滤 |
B | NaCl溶液(Br2) | 乙醇 | 分液 |
C | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
D | KNO3溶液(KOH) | FeCl3溶液 | 过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用甲苯生产对-羟基苯甲酸乙酯:![]() ,下列反应①—⑥是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
,下列反应①—⑥是其合成过程,其中某些反应条件及部分反应物或生成物未注明。
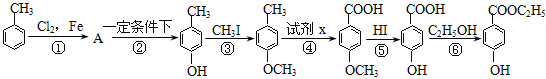
回答下列问题:
(1)有机物A的结构简式为___________________。A的名称为 。
(2)反应①的化学方程式是:____________________________________。
(3)试剂x是___________。
(4)反应⑥的化学方程式是:_____________________________________。
(5)合成路线中设计③、⑤两步反应的目的是_____________
(6)CH3O-![]() -COOH的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有 种,其中核磁共振氢谱为5组峰,且峰面积比为2∶2∶2∶1∶1的为 (写结构简式)。
-COOH的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有 种,其中核磁共振氢谱为5组峰,且峰面积比为2∶2∶2∶1∶1的为 (写结构简式)。
(7)已知:![]() ,写出以苯酚和乙醇为原料制备
,写出以苯酚和乙醇为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中的实验装置可用于制取乙炔。请填空:

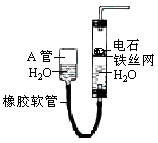
(1)图中,A管的作用是 。制取乙炔的化学方程式是 。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是 ,乙炔发生了 反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象是 , 乙炔发生了 反应。
(4)为了安全,点燃乙炔前应 ,乙炔燃烧时的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下表中各项的排布规律,按此规律排布第23项应为( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C2H6 | C2H4 | C2H4O2 | C3H8 | C3H6 | C3H6O2 | C4H10 | C4H8 | C4H8O2 | C5H12 |
A.C9H18 B.C9H118O2 C.C8H18 D.C8H16O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】理论上下列反应不能设计成原电池反应的是
A.2Fe3+ + Cu = 2Fe2+ + Cu2+
B.Zn + 2H+ = Zn2+ + H2↑
C.2H2 + O2 = 2H2O
D.H+ + OH- = H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子结构和元素周期律的表述正确的是
A. 氮的非金属性比磷强,所以氮气的性质比白磷活泼
B. ⅦA族元素一定是同周期中非金属性最强的元素
C. IA族元素的金属性一定比IIA族元素的金属性强
D. Na+半径大于Cl﹣半径
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com