


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
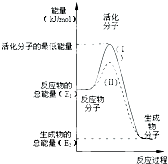 (1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、红棕色先变浅后变深最终颜色较浅 |
| B、红棕色先变浅后变深最终颜色较深 |
| C、红棕色先变深后再变浅最终颜色较浅 |
| D、红棕色先变深后变浅最终颜色较深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
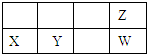
A、X离子结构示意图: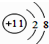 |
| B、原子半径Y比Z大 |
| C、元素的气态氢化物的稳定性Z强于W |
| D、X和Y两元素的最高价氧化物的对应水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取25.20gNaCl |
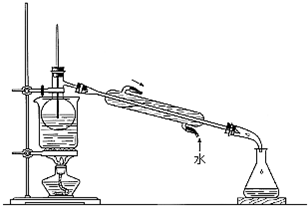
| B、用四氯化碳萃取碘的饱和水溶液中的碘分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出. |
| C、在蒸发皿中放入NaCl溶液,加热、蒸发制取NaCl晶体 |
| D、用100mL容量瓶配制50mL0.1mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
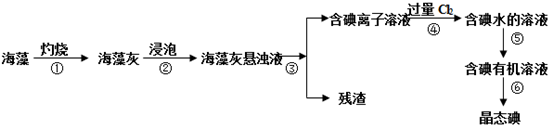
| A、①②③④ | B、②③④① |
| C、②③①④ | D、③②④① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com