

分析 A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,可知A为Na,B为Al,E的最外层电子数为10-1-3=6,可知E为S元素,C元素的最外层电子数比次外层电子数少4,C为Si元素;D元素原子次外层电子数比最外层电子数多3,D为P,以此来解答.
解答 解:(1)由上述分析可知,B为Al,C为Si,E为S,故答案为:Al;Si;S;
(2)A与E两元素可形成化合物为Na2S,用电子式表示其化合物的形成过程为 ,
,
故答案为: ;
;
(3)A、B两元素的最高价氧化物的水化物之间的相互反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:Al(OH)3+NaOH=NaAlO2+2H2O;
(4)非金属性P>Si,C、D的最高价氧化物的水化物的酸性为H3PO4>H2SiO4,故答案为:H3PO4>H2SiO4.
点评 本题考查位置、结构与性质,为高频考点,把握原子结构、元素化合物知识推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:推断题
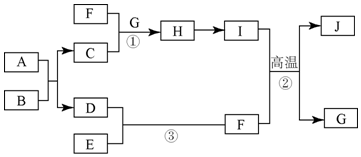
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ①②④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 操作及现象 |
| i | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
| ii | 向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以淀粉为原料可以制取乙酸乙酯 | |
| B. | 福尔马林可用于浸制标本,是因为其能使蛋白质变性 | |
| C. | 医用酒精通常是指体积分数为75%的乙醇溶液 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液Na+、K+、MnO4-、Fe2+ | B. | 酸性溶液Fe3+、NH4+、SCN-、NH3+ | ||
| C. | 碱性溶液Na+、K+、AlO2-、SO42- | D. | 碱性溶液Ba2+、Na+、HCO3-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com