
| A. | Na2S2O3是还原剂 | |
| B. | 根据该反应可判断氧化性:Cl2>SO42-、 | |
| C. | □的物质是HCl | |
| D. | 上述反应中,每生成1mol SO42-,转移2mole- |
分析 由原子及电子守恒可知,反应为4Cl2+Na2S2O3+5H2O=2NaCl+2H2SO4+6HCl,S元素的化合价由+2价升高为+6价,Cl元素的化合价由0降低为-1价,以此来解答.
解答 解:由原子及电子守恒可知,反应为4Cl2+Na2S2O3+5H2O=2NaCl+2H2SO4+6HCl,
A.S元素的化合价升高,Na2S2O3是还原剂,故A正确;
B.Cl2为氧化剂,H2SO4是氧化产物,由氧化剂的氧化性大于氧化产物的氧化性可知氧化性:Cl2>SO42-,故B正确;
C.由原子守恒可知□的物质是HCl,故C正确;
D.上述反应中,每生成1mol SO42-,转移1mol×(6-2)=4mole-,故D错误;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ | |
| C. | 硝酸银溶液中加入铜粉:Ag++Cu═Cu2++Ag↓ | |
| D. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,分子总数为NA的H2和O2混合气体,其体积约为22.4L | |
| B. | 5.6g铁与足量的氯气反应,转移电子数为0.2NA | |
| C. | 11.2LH2O所含有的原子数为1.5NA | |
| D. | 0.2mol/L的Na2CO3溶液中含有的Na+数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.8 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.8 mol |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
可逆反应2SO2(g)+O2(g)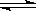 2SO3(g)从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是( )
2SO3(g)从正方向开始,并达到了平衡。此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是( )
A .新平衡体系中,SO2和O2物质的量之比仍为2∶1
B .平衡向正反应方向移动了,原因是正反应速率增大了,逆反应速率减小了
C .新平衡体系与旧平衡体系比较,SO3的浓度肯定增大了
D .若采取的措施是缩小容器的容积,则新旧平衡中SO2和O2的转化率之比都是1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
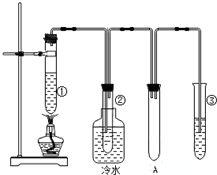 石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已忽略).在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水.
石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已忽略).在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水.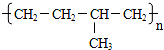 B.
B.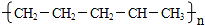
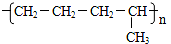 D.
D.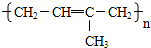
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X单质在一定条件下能与Z的最高价氧化物发生置换反应 | |
| B. | 原子半径:Y>Z>W | |
| C. | 最高价氧化物对应水化物的酸性由弱到强的顺序:X<Z<W | |
| D. | 室温下,0.1mol/LW的气态氢化物的水溶液的pH=1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com