
| A. | 单质 | B. | 混合物 | C. | 无机物 | D. | 有机物 |
科目:高中化学 来源: 题型:解答题
 ,在Na、Al、Fe三种金属元素中,其所形成氧化物种类最多的元素是Fe,所形成的氧化物中适宜做耐火材料的元素是Al;
,在Na、Al、Fe三种金属元素中,其所形成氧化物种类最多的元素是Fe,所形成的氧化物中适宜做耐火材料的元素是Al;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
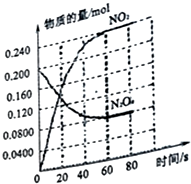 在容积为2.0L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体颜色变深.回答下列问题:
在容积为2.0L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体颜色变深.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 强电解质 | AgCl | SO3 | 醋酸 | 熔融NaOH |
| 弱电解质 | 晶体桂 | BaSO4 | HF | Fe(OH)3 |
| 非电解质 | CH4 | 液氨 | C2H5OH | C02 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a、b不可能是同种材料的电极 | |
| B. | 该装置可能是原电池,也可能是电解池 | |
| C. | 该装置可能是原电池,电解质溶液为稀硝酸 | |
| D. | 该装置的电极可以是铜锌,电解质溶液是稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋可同时用作防腐剂和调味剂 | |
| B. | 食品添加剂必须用天然物质制造 | |
| C. | 柠檬黄常用作着色剂,改善食品色泽 | |
| D. | 食品添加剂在合理限量范围内使用是可以的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 试管 | 操作 | 现象 |
| 1 | 加入碘水 | 溶液变成蓝色 |
| 2 | 加入银氨溶液,水浴加热 | 未出现银镜 |
| 3 | 加入碘水 | 溶液变成蓝色 |
| 4 | 加入银氨溶液,水浴加热 | 未出现银镜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,33.6 LSO3中含有氟原子的数目为1.5NA | |
| B. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| C. | 7.8 g Na2O2中含有的阴离子数为0.2NA | |
| D. | 1 molCl2参加反应转移电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
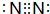 ;构成AlN的微粒是Al原子和N原子.
;构成AlN的微粒是Al原子和N原子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com