
| A. | 糖类和蛋白质都是人体重要的营养物质 | |
| B. | 蛋白质在一定条件下能发生水解反应,生成氨基酸 | |
| C. | 加热能杀死甲型H1N1流感病毒,因为病毒的蛋白质受热变性 | |
| D. | 蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,如再加水也不溶解 |
分析 A.人类重要的营养物质包含糖类、油脂、蛋白质、维生素、无机盐和水;
B.蛋白质含-CONH-;
C.高温下蛋白质发生变性;
D.蛋白质溶液中加入饱和硫酸铵溶液,发生盐析,为可逆过程.
解答 解:A.糖类和蛋白质都是人体重要的营养物质,为生命活动提供能量,故A正确;
B.蛋白质含-CONH-,在一定条件下能发生水解反应,生成氨基酸,故B正确;
C.病毒的成分为蛋白质,加热能杀死甲型H1N1流感病毒,因为病毒的蛋白质受热变性,故C正确;
D.蛋白质溶液中加入饱和硫酸铵溶液,发生盐析,为可逆过程,则蛋白质析出,如再加水又溶解,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意基本营养物质的结构与性质,题目难度不大.


科目:高中化学 来源: 题型:解答题
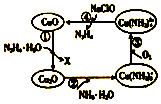 水合肼(N2H4•H2O)又称水合联氨,其纯净物为无色透明的油状液体,具有强碱性和吸湿性.将水合肼通入CuO胶体中,可发生如图所示的转化.
水合肼(N2H4•H2O)又称水合联氨,其纯净物为无色透明的油状液体,具有强碱性和吸湿性.将水合肼通入CuO胶体中,可发生如图所示的转化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2O7、P2O5、SO3、CO2均属于酸性氧化物 | |
| B. | Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物 | |
| C. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 | |
| D. | 根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q2<Q1<197 kJ•mol-1 | B. | Q2=Q1=197 kJ•mol-1 | ||
| C. | Q1<Q2<197 kJ•mol-1 | D. | Q2=Q1<197 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
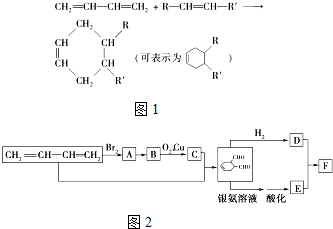
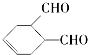 中含氧官能团的名称是醛基
中含氧官能团的名称是醛基 OHCCH=CHCHO+2H2O.
OHCCH=CHCHO+2H2O. .
. 、HC≡CCOOCH3.
、HC≡CCOOCH3.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氧化还原反应中,阴离子只能发生氧化反应 | |
| B. | 碳酸钠溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 有些吸热反应不需要加热也能进行 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
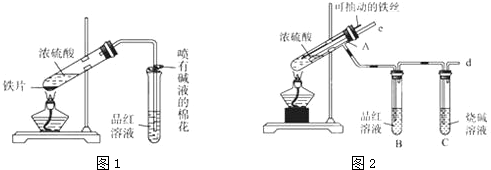
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com