
【题目】NA为阿伏加德罗常数的值。参阅表中数据,下列判断在标准状况下正确的是
NO2 | HF | |
熔点/℃ | -11.2 | -83.6 |
沸点/℃ | 21.0 | 19.52 |
A. 2.0gHF中含电子数目为l.0NA
B. 12g石墨烯(单层石墨)中含有六元环个数为NA
C. 6.72LNO2与水反应后,转移的电子数为0.2NA
D. NO和O2各2.24L充分反应后所得混合物体系中含分子数为0.1NA
【答案】A
【解析】由表中数据可知,二氧化氮和氟化氢的沸点分别为21.0℃和19.52℃,所以在标准状况下,二氧化氮和氟化氢都是液体。A. HF分子中有10个电子,相对分子质量为20,所以2.0gHF的物质的量为0.1mol,所含电子的物质的量为1mol,所以电子的数目为1.0NA,A正确;B. 在石墨烯中,每个六元环中有6个碳原子,每个碳原子参与3个六元环,所以平均每个六元环占有碳原子数为6![]() 。12g石墨烯含碳原子的物质的量是1mol,所以含有六元环个数为0.5NA,B不正确;C. 无法计算6.72LNO2的物质的量,所以无法计算与水反应后转移的电子数,C不正确;D. 同样无法计算NO和O2的物质的量,当然也无法计算充分反应后所得混合物体系中含分子数,D不正确。本题选A。
。12g石墨烯含碳原子的物质的量是1mol,所以含有六元环个数为0.5NA,B不正确;C. 无法计算6.72LNO2的物质的量,所以无法计算与水反应后转移的电子数,C不正确;D. 同样无法计算NO和O2的物质的量,当然也无法计算充分反应后所得混合物体系中含分子数,D不正确。本题选A。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是
A. 1 mol FeI2与足量氯气反应时转移的电子数为2NA
B. 常温常压下,46gNO2和N2O4混合气体含有的原子数为3NA
C. 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子数为0.4 NA
D. 常温下56 g铁片投入足量浓H2SO4中生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应。已知钠及其氧化物的物质的量均为0.lmol,水的质量为100g。下列说法正确的是

A. Na2O2中阴阳离子数目之比为1:1
B. 反应①的离子方程式为:Na+2H2O=Na++2OH-+H2↑
C. 反应③最多能产生0.05molO2
D. ①、②、③充分反应后所得溶液的质量分数从大到小:①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn与稀HNO3反应的物质的量之比为5:12,氧化产物为硝酸锌,则HNO3被还原的产物为( )
A. NOB. NO2C. N2D. N2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法能达到实验目的的是
A.用丁达尔效应鉴别淀粉胶体和蛋白质胶体
B.用加热的方法除去NaCl固体中的NH4Cl
C.用BaCl2溶液鉴别Na2SO4溶液和AgNO3溶液
D.用饱和Na2CO3溶液除去CO2中的HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色废水中可能含有NH4+、Fe3+、Al3+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,进行了如下三组实验:
①取溶液做焰色反应,火焰为黄色
②取废水样品l00mL,依次加足量的BaCl2溶液和稀HC1,得白色沉淀23.3g
③另取废水样品l00mL向其中加入Na2O2固体,产生的沉淀和气体与所加Na2O2固体物质的量的关系曲线如图

请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有:________________。
(2)写出图象中沉淀溶解阶段发生的离子反应方程式:_________________、____________________。
(3)根据图象分析可知,在原溶液中一定存在的阳离子及其物质的量比值为____________。
(4) NO3-是否存在?_____________; (填“存在‘不存在”或“不确定”)若存在其物质的量浓度为_________________。(若不存在或不确定,该空不填)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
如图为实验室某浓硫酸试剂瓶的标签,试根据标签上的有关数据回答下列问题: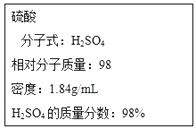
(1)该浓硫酸中H2SO4的物质的量浓度为
(2)某学生欲用上述浓硫酸和蒸馏水配制250mL物质的量浓度为0.4molL﹣1的稀硫酸,该学生需要量取上述浓硫酸进行配制.
(3)为配制(2)中的稀硫酸,下列可供选用的仪器中,一定用到的是(填编号),配制过程中还缺少的仪器是(填写仪器名称)
①玻璃棒;②胶头滴管;③量筒;④药匙;⑤圆底烧瓶;⑥天平;⑦烧杯;⑧普通漏斗
(4)取上述配制好的硫酸溶液50mL与足量的铝反应,所得溶液中c(Al3+)=(忽略溶液体积的变化),检验溶液中SO42﹣存在的方法:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 氨气易液化,液氨气化时吸热,因此液氨常用作制冷剂
B. 氮的固定是指将游离态的氮转变为氮的化合物
C. 漂白粉和漂粉精的有效成分都是Ca(ClO)2
D. SO2和CO2都是造成酸雨的主要气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com