
【题目】下列说法正确的是( )
A.分子式为C2H6O的有机化合物性质相同
B.相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能途径a:C![]() CO+H2
CO+H2![]() CO2+H2O 途径b:C
CO2+H2O 途径b:C![]() CO2
CO2
C.食物中可加入适量的食品添加剂,如香肠中可以加少量的亚硝酸钠以保持肉质新鲜
D.生石灰、铁粉、硅胶是食品包装中常用的干燥剂
科目:高中化学 来源: 题型:
【题目】反应COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④B.①④⑥C.②③⑤D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

(1)氢氧燃料电池的能量转化主要形式是___,在导线中电子流动方向为___(用a、b和箭头表示)。
(2)正极反应的电极反应方程式为___。
(3)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

①图1中N型半导体为___(填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___。
③若A极产生7.00gN2,则此时B极产生___LH2(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2A(g)+B(g)![]() 3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
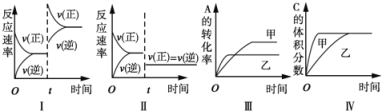
A. 图I表示增加反应物浓度对该平衡的影响
B. 图II表示减小压强对该平衡的影响
C. 图Ⅲ表示温度对该平衡的影响,温度:乙>甲
D. 图IV表示催化剂对该平衡的影响,催化效率:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知空气组成(体积分数)N2:0.800,O2:0.200,氨空气氧化后的混合气体组成如下(高温下NO与O2可以共存)NO:16 mol;O2:7.00 mol;H2O:24.5 mol;N2:112 mol。
完成下列计算:
(1)该混合气体中NO全部转化为HNO3,需要___________摩尔O2 。
(2)参加反应的空气的体积是___________升。(标准状况下)
(3)向该混合气体中添加空气使NO完全转化为 HNO3,转化后剩余气体中(不含H2O)氧气体积分数为0.0500。添加空气多少摩尔?___________
(4)该混合气体的组成表明NH3氧化产生的NO超过16 mol,有部分NO已和O2、H2O 反应转化为HNO3。这部分NO是多少摩尔? _______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
B. Na2CO3溶液中CO32-的水解:CO32-+H2O=HCO3-+OH-
C. 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O
D. NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一容积为2 L的密闭容器内,加入0.8 mol H2和0.6 mol I2,在一定条件下发生反应:H2(g)+I2(g)2HI(g)ΔH<0。反应中各物质的物质的量随时间变化情况如图:
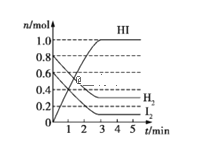
(1)该反应的化学平衡常数表达式为______,若升高温度,化学平衡常数K______(填“增大”、“减小”或“不变”)。
(2)根据图中数据,反应开始至达到平衡时,平均速率v(HI)=_____mol·L-1·min-1,转化率α(H2)=_____。
(3)HI的体积分数φ(HI)随时间变化如图中曲线Ⅱ所示。若改变反应条件,在甲条件下φ(HI)的变化如图中曲线Ⅰ所示,在乙条件下φ(HI)的变化如图中曲线Ⅲ所示。则甲条件可能是_____(填入下列条件的序号,下同),乙条件可能是______。
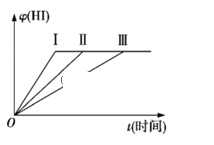
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温恒容条件下,加入适当催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有甲、乙、丙三瓶等体积的新制的氯水,浓度均为0.1molL-1。如果在甲瓶中加入少量的NaHCO3晶体(mmol),在乙瓶中加入少量NaHSO3(mmol),丙瓶不变,片刻后甲、乙、丙三瓶溶液中HClO的物质的量的浓度大小关系是(溶液体积变化忽略不计)( )
A.甲=乙>丙B.甲>乙>丙C.丙>甲=乙D.甲>丙>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00 L的密闭容器中,充入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随着温度升高,混合气体的颜色变深。体系中各物质的浓度变化与时间关系如图所示。下列说法正确的是
2NO2(g),随着温度升高,混合气体的颜色变深。体系中各物质的浓度变化与时间关系如图所示。下列说法正确的是

A.反应的△H <0
B.在 060s 时段,反应速率v(N2O4)=0.001mol·L-1·s-1
C.平衡时,反应的平衡常数K=0.240
D.T1℃时平衡后将温度变为T2℃,测得c(N2O4)降低,则T1>T2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com