
下列说法正确的是
A.乙醇的酯化反应、甲苯的硝化反应以及酯的水解均属于取代反应
B.乙烷生成溴乙烷和乙烯生成溴乙烷的反应类型相同
C.可用氢氧化钠溶液除去乙酸乙酯中混有的乙酸和乙醇
D.蛋白质、淀粉、纤维素、油脂均属于天然高分子化合物,均能发生水解反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称氢化物。下列物质不属于氢化物的是( )。
A.H2O B.H2SO4 C.NaH D.NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
绿原酸是咖啡提取液成分之一,下列关于绿原酸的说法正确的是( )
 A.水解产物都可以与FeCl3溶液发生显色反应
A.水解产物都可以与FeCl3溶液发生显色反应
B.一定条件下,1 mol该物质最多与4 molNaOH反应
C. 分子中所有碳原子可能共面
D.1 mol该物质最多与含6 mol Br2的浓溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明的酸性溶液中能大量共存的一组离子是
A. NH4+ 、NO3-、Fe2+、Cl- B.Na+、CH3COO-、K+、SO42-
C.MnO4-、K+、SO42-、Na D. Mg2+、Al3+、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
有5瓶白色固体试剂,分别是Ba(NO3)2 、KCl、 NaOH.、CuSO4.、Na2SO 4,现只提供蒸馏水,通过下面的实验步骤可鉴别它们。请填写下列空白:
4,现只提供蒸馏水,通过下面的实验步骤可鉴别它们。请填写下列空白:
⑴ 各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象
是 ,被检出的物质的化学式是 。
⑵ 分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象和相应的化学方程
式:①现象:试管中有白色沉淀生成,离子方程式:
②现象:试管中有蓝色沉淀生成,化学方程式: ;
由上述两个现象可知,被检验出的物质的化学式是 和
(3用⑵检测出 可以鉴别剩余的两种物质。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+O2(g) 2SO3(g) ΔH<0
2SO3(g) ΔH<0
(1)写出该反应的化学平衡常数表达式K=_________________________。
(2)降低温度,该反应K______,二氧化硫转化率________,化学反应速率________(填“增大”、“减小”或“不变”)。
(3)600 ℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3的物质的量变化如图,反应处于平衡状态的时间___________________。
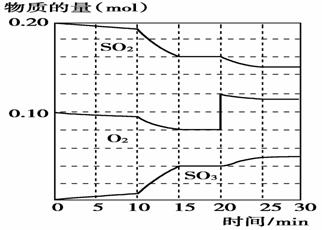
(4)据图判断,反应进行至20 min 时,曲线发生变化的原因是(用文字表达)________________________ _____________ __;
10 min到15 min时曲线变化的原因可能是(填写编号)________。
a.加了催化剂 b.缩小了容器体积 c.降低温度 d.增加SO3的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是短周期元素,其部分性质如下表
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的2/3 |
| Z | 第三周期原子半径最小的金属 |
下列说法正确的是
A.气态氢化物的热稳定性:X>W
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.Z的氧化物中含有非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
进入2013年以来,我国中东部地区多次遭遇大范围、长时间的雾霾天气。车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。
(1)活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
|
T/℃ n/mol | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.10 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
①结合上表数据,写出NO与活性炭反应的化学方程式 。
②上述反应T1℃时的平衡常数K1= 。
③根据上述信息判断,温度T1和T2的关系是(填序号) 。
a.T1>T2 b.T1<T2 c.无法比较
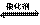 (2)车辆排放的氮氧化物和碳氧化物在催化剂作用下可发生反应:
(2)车辆排放的氮氧化物和碳氧化物在催化剂作用下可发生反应:
2CO+2NO N2+2CO2 在一体积为1L的密闭容积中,加入0.40mol的CO和0.40mol的NO ,反应中N2的物质的量浓度的变化情况如图所示,回答下列问题。
①计算从反应开始到平衡时,平均反应速率v(N2)= 。
②在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时N2的浓度约为
0.25 mol/L)。请在上图中画出第5分钟末到此平衡时N2浓度的变化曲线。
(3)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,在一定条件下,用CH4还原NOX可以消除氮氧化物的污染。
 例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
2NO2(g) N2O4(g) △H=-56.9 kJ/mol
写出CH4还原N2O4(g)生成N2和H2O(g)的热化学方程式 。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放目的。通过人工光合作用,以CO2和H2O为原
料可以制备HCOOH和O2,计算标况下每回收1.0m3 CO2转移的电子数为 个。
③常温下,0.1mol/L的HCOONa溶液的pH为10,则HCOOH的电离常数Ka = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在标准状况下的四种气体 ①6.72L CH4 ;②3.01×1023个HCl分子;③13.6克H2S ; ④0.2molNH3 该条件下体积最大和含氢原子数最多的依次是
A.②和① B.②和④ C.①和④ D.③和①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com