
【题目】下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。

(1)上述元素中单质的熔点最高的可能是________(填名称)。
(2)比较D、G氢化物的稳定性 (用化学式表示)。
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为: ;
(4)D、E、G、H四种元素最高价含氧酸的酸性由强到弱的顺序是: (填化学式)。
(5)A、D两种元素构成的两种烃X和Y,X是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;Y是一种比水轻的油状液体,两种元素的质量比为12∶1,Y的相对分子质量为78。
①X的结构简式 。
②Y与浓硫酸与浓硝酸在50~60℃反应的化学反应方程式: ,反应类型________。
【答案】(1)碳
(2)CH4﹥SiH4
(3)![]()
(4)HClO4﹥HNO3﹥H2CO3﹥H2SiO3
(5)①CH2=CH2
② C6H6+HNO3![]() C6H5NO2+H2O;取代反应(硝化反应)
C6H5NO2+H2O;取代反应(硝化反应)
【解析】试题分析:图中所示为元素周期表中短周期元素的一部分,根据各元素在周期表中的位置可以推知:A为氢元素、B为氦元素、C为钠元素、D为碳元素、E为氮元素、F为氧元素、G为硅元素、H为氯元素。据此可得下列结论:
(1)上述元素中单质的熔点最高的可能是碳。
故答案为:碳;
(2)元素的非金属性越强,形成气态氢化物越稳定。D为碳元素、G为硅元素,非金属性D>G,所以氢化物的稳定性CH4﹥SiH4。
故答案为:CH4﹥SiH4;
(3)A为氢元素、E为氮元素,在一定条件下,A与E可形成一种极易溶于水的气态化合物为氨气,其电子式为:![]() ;
;
故答案为:![]() ;
;
(4)元素的非金属性越强,其最高价氧化物对应的水化物酸性越强,D为碳元素、E
为氮元素、G为硅元素、H为氯元素,非金属性: Cl﹥N﹥C﹥Si,所以四种元素最高价含氧酸的酸性由强到弱的顺序是:HClO4﹥HNO3﹥H2CO3﹥H2SiO3。
故答案为:HClO4﹥HNO3﹥H2CO3﹥H2SiO3;
(5)A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平,则A为CH2=CH2;B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,则原子个数之比为1:1,符合CnH2n-6,B的相对分子质量为78,则12n+2n-6=78,解得n=6,所以B为苯。
①A为乙烯,结构简式为:CH2=CH2。
故答案为:CH2=CH2;
②B与浓H2SO4与浓HNO3在50-60℃反应的化学反应方程为:C6H6+HNO3![]() C6H5NO2+H2O,属于取代反应。
C6H5NO2+H2O,属于取代反应。
故答案为:C6H6+HNO3![]() C6H5NO2+H2O;;取代反应。
C6H5NO2+H2O;;取代反应。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
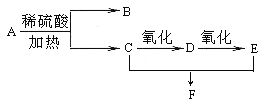
【题目】化合物A的分子式为C3H6O2,它有如下图所示转化关系,已知D、E、F在加热条件下都能与碱性新制Cu(OH)2悬浊液生成砖红色沉淀:
试回答下列问题:
(1)A的名称为 ,B所含官能团的名称为 ;
(2)写出A 生成B、C的化学反应方程式: ,
(3)写出C催化氧化为D的化学反应方程式: ;
(4)写出C和E生成F的化学反应方程式: ,反应类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
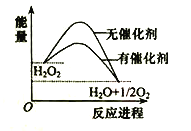
A. 加入催化剂,减小了反应的热效应
B. 加入催化剂,可提高H2O2的平衡转化率
C. H2O2分解的热化学方程式:H2O2 → H2O + O2 + Q
D. 反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的除杂方案正确的是
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | CO2(g) | SO2(g) | 饱和Na2CO3溶液、浓H2SO4 | 洗气 |
B | NH4Cl(ap) | Fe3+(ap) | NaOH溶液 | 过滤 |
C | NaCl(s) | KNO3(g) | AgNO3溶液 | 过滤 |
D | Cu(s) | Ag(s) | CuSO4 | 电解法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄酮醋酸(F)具有独特抗癌活性,它的合成路线如下:
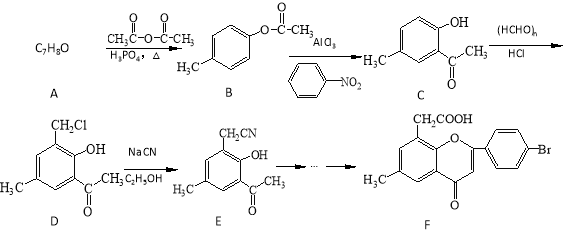
![]() 已知:RCN在酸性条件下发生水解反应:
已知:RCN在酸性条件下发生水解反应:![]()
(1)已知A转化为B的同时还生成了乙酸,则A的结构简式为 ,该反应类型是 。
(2)C的分子式为 。
(3)F分子中有3个含氧官能团,名称分别为醚键、 和 。
(4)写出B与过量氢氧化钠水溶液反应的化学方程式(不必注明反应条件): 。
(5)写出两个符合下列条件的C的同分异构体的结构简式 、 。
①能与NaHCO3反应生成CO2 ②苯环上有两种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物不能由CH2=CH2通过加成反应制取的是
A.CH3CH2Cl B.CH2Cl—CH2Cl C.CH3—CH3OH D.CH3—COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一容积不变的密闭容器中,充入一定量HI气体,发生如下可逆反应:
2HI(g)![]() H2(g)+I2(g)ΔH>0。下列说法正确的是( )
H2(g)+I2(g)ΔH>0。下列说法正确的是( )
A.若每消耗2n mol HI的同时生成n mol H2,表明该反应已达平衡
B.容器内的压强不发生变化,表明该反应已达平衡
C.平衡时,若其他条件不变,再充入一定量HI,重新达平衡后,I2的百分含量增大
D.平衡时,若其他条件不变,升高温度,混合气体的颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 ==2CO2 +3H2O,电池示意如图,下列说法不正确的是
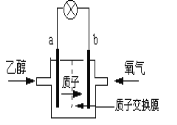
A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池工作时,1mol乙醇被还原时就有6mol电子转移
D.电池正极的电极反应为:4H+ + O2 + 4e— =2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明ClO2具有 性。
(2)工业上可以通过下列方法制取ClO2,请完成该反应化学方程式:
2KClO3+ SO2 = 2ClO2 + 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com