
���� A���ʵ�����ʺɱ�Ϊ46������Է�������Ϊ46���������ͼ���ִ���C=O����C-O���Ȼ�ѧ���������գ�˵���л��������������2��Oԭ�ӡ�1��Cԭ�ӣ���ȥ��2��Oԭ�ӡ�1��Cԭ�Ӻ�ʣ����ʽ��Ϊ46-16��2-12=2����Ϊ2��Hԭ�ӣ�A�ķ���ʽΪCH2O2���˴Ź������ױ�����A���ʺ˴Ź���������������ԭ�����շ壬�ҷ����֮��Ϊ1��1������֪AΪHCOOH��
��� �⣺A���ʵ�����ʺɱ�Ϊ46������Է�������Ϊ46���������ͼ���ִ���C=O����C-O���Ȼ�ѧ���������գ�˵���л��������������2��Oԭ�ӡ�1��Cԭ�ӣ���ȥ��2��Oԭ�ӡ�1��Cԭ�Ӻ�ʣ����ʽ��Ϊ46-16��2-12=2����Ϊ2��Hԭ�ӣ�A�ķ���ʽΪCH2O2���˴Ź������ױ�����A���ʺ˴Ź���������������ԭ�����շ壬�ҷ����֮��Ϊ1��1������֪AΪHCOOH��
��1������ʱ���������ܡ�ţ�ǹܡ���ƿ���ƾ��ơ��¶ȼ��⣬���õ��IJ��������ǣ�������ƿ��
�ʴ�Ϊ��������ƿ��
��2��A���ʵĽṹ��ʽ��HCOOH�������ŵ����ƣ��Ȼ���
�ʴ�Ϊ��HCOOH���Ȼ���
��3����ȷ��A�Ľṹ���о���ѧϰС�����A���ܾ������ԣ���֤A������ʵ�鷽�����μ���ɫʯ����Һ��죬
�ʴ�Ϊ���μ���ɫʯ����Һ��죮
���� ���⿼���л������ʽ��ṹ��ȷ�������ؿ���ѧ�����������������ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������кܸߵ��۷е� | B�� | �������ǽ������� | ||
| C�� | �������л��� | D�� | ���������Ӿ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ���������ڵ��� | B�� | Ư��Һ��ʯӢ�����ڴ����� | ||
| C�� | ����ռ�Ǽ� | D�� | ���ǡ������ʶ����ڸ߷��ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
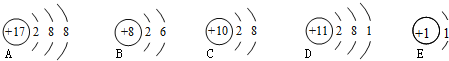
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ƽ�Ĺ��չ�����Ӧ���������ܽ�ȵIJ��� | |
| B�� | ��ҵ����������ʯ����Ϊԭ���Ʊ�Ư�� | |
| C�� | ���ʹ賣�������ά�IJ��ϣ������İ뵼��������һ����ϵ | |
| D�� | ��ѹ�ƵƷ����Ļƹ����Զ��������ǿ��������·�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ��ͬѹ�£���ͬ������κ����ʣ������ʵ���һ����� | |
| B�� | ��������SO2��SO3��������ԭ������� | |
| C�� | 1L����һ����1L����������С | |
| D�� | �κ������£������ʵ����ļ����һ����̼�����ķ�����һ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��2Cu+O2 $\frac{\underline{\;��\;}}{\;}$2CuO���Ƴ�Cu+S$\frac{\underline{\;��\;}}{\;}$CuS | |
| B�� | SO2�������������SO3Ҳ������������ | |
| C�� | ��ͬ������N4��N2����ԭ�Ӹ�����Ϊ1��1 | |
| D�� | ʯī�����ʯ��C60Ϊͬ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
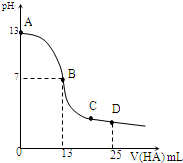 �����£���25mL 0.1mol/L MOH��Һ����μ���0.2mol/L HA��Һ��������ͼ��ʾ������仯���Բ��ƣ����ش��������⣺
�����£���25mL 0.1mol/L MOH��Һ����μ���0.2mol/L HA��Һ��������ͼ��ʾ������仯���Բ��ƣ����ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com