
在绿色化学工艺中,理想状态是反应物中的原子全部转化为欲制得的产物。如用CH3C≡CH合成CH2=C(CH3)COOCH3,欲使原子利用率达到最高,还需要的反应物是
A. H2和CO2 B.CO2和H2O C.CO和CH3OH D.CH3OH和H2
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1 L 0.1 mol/L Na2CO3溶液中,阴离子总数大于0.1 NA
B.常温常压下,1 mol甘氨酸中含C—H键数目为3 NA
C.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1 NA
D.50℃时,10 L pH = 13的NaOH溶液中含有的OH—数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于乙酸性质的叙述中,错误的是 ( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体
B.乙酸具有氧化性,能跟钠反应放出H2
C.乙酸分子中含有碳氧双键,所以它能使溴水褪色
D.乙酸在温度低于16.6℃时,就凝结成冰状晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同。A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)A元素单质的化学式为______________________,D元素的原子结构示意图为____________________________。
(2)由A、B、C三种元素形成的化合物的电子式为_______________,这种化合物中所含的化学键类型有______________________________________。
(3)A2B的沸点高于A2D,其原因是______________________________________。
(4)B、C、E三种元素形成一种盐,此盐中三种原子个数比为1∶1∶1,在25 ℃时,将该盐溶于水,测得溶液pH>7,理由是_________________(用离子方程式表示);将该盐溶液在空气中露置一段时间后(充分光照,不考虑水分的挥发),溶液的pH近似为7,则该过程的总反应方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用有机物分子内基团间的相互作用解释的是
A.乙烯能发生加成反应而乙烷不能
B.苯酚(C6H5OH)能跟NaOH溶液反应而乙醇不能
C.甲苯能使KMnO4酸性溶液褪色而乙烷不能
D.苯在50℃~ 60℃时发生硝化反应而甲苯在30℃时即可
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列几种物质:
①CaS ②Ar ③CaO2 ④金刚石 ⑤SiC ⑥H2O2 ⑦(NH4)2SO4 ⑧MgCl2 ⑨CH3COONa ⑩[Cu(NH3)4]SO4 (以下空格均填写序号)
(1)不含极性键的分子晶体是 ;(2)含有极性键的分子晶体是 ;
(3)只含离子键的离子晶体是 ;(4)含有极性键的原子晶体是 ;
(5)含有非极性键的离子晶体是 ;(6)含有配位键的离子晶体是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
人类生活需要能量。下列能量主要由化学变化产生的是 ( )。
A.电熨斗通电发出的热量
B.电灯通电发出的光
C.水电站利用水力产生的电能
D.液化石油气燃烧放出的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷在不同条件下有两种热解反应:①CH4(g)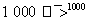 C(s)+2H2(g);②2CH4(g)
C(s)+2H2(g);②2CH4(g)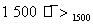 C2H2(g)+3H2(g)。现将两份标准状况下等体积的甲烷分别通入两个容积可变的密闭容器中,按①式和②式热解,待完全反应后,恢复至标准状况,则两容器中气体体积关系正确的是 ( )。
C2H2(g)+3H2(g)。现将两份标准状况下等体积的甲烷分别通入两个容积可变的密闭容器中,按①式和②式热解,待完全反应后,恢复至标准状况,则两容器中气体体积关系正确的是 ( )。
A.①和②相等 B.①小于②
C.①大于② D .无法判断
.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
关于宝石的性质,下列说法正确的是 ( )。
A.金刚石是自然界中最坚硬的物质
B.刚玉的主要化学成分是SiO2
C.珍珠的主要成分是CaCO3和有机化合物
D.红宝石中含有微量元素Cu,蓝宝石中含有微量元素Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com