
| A、ZnC2水解生成乙炔C2H2 |
| B、Al4C3水解生成丙炔C3H4 |
| C、Mg2C3水解生成丙烯C3H6 |
| D、Li2C2水解生成乙烯C2H4 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、少量浓硫酸溅到皮肤上,立即用氢氧化钠溶液冲洗 |
| B、大量氯气泄漏时,可用肥皂水浸湿毛巾捂住口和鼻,并迅速离开现场 |
| C、金属镁着火,用干粉灭火器扑灭 |
| D、金属钠着火用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠浮于液面,到处游动,发出嘶嘶响声 |
| B、溶液中溶质的质量增大,并放出H2 |
| C、溶液中NaOH的质量分数不变,有H2放出 |
| D、溶液的质量减少,有H2放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、向NaAlO2溶液中通入足量的CO2:AlO
| ||||
B、(NH4)2Fe(SO4)2溶液中加入过量的氢氧化钡溶液:2NH
| ||||
C、NaHSO4溶液中加入Ba(OH)2溶液至溶液呈中性:Ba2++OH-+H++SO
| ||||
D、用惰性电极电解NaHS溶液:S2-+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 燃料 | H2 | CH4 | C2H2 | C2H5OH |
| 燃烧热△H/KJ.mol-1 | -285.8 | -890.3 | -1299.6 | -1366.8 |
| A、H2 |
| B、CH4 |
| C、C2H2 |
| D、C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
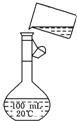 电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有泥沙、Ca2+、Mg2+、Fe3+、SO
电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有泥沙、Ca2+、Mg2+、Fe3+、SO2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 酶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
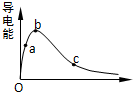 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com