
| A. | 该晶体属于离子晶体,M呈+2价 | |
| B. | 该晶体属于分子晶体,化学式为MFe2(CN)6 | |
| C. | 该晶体中与每个Fe3+距离相等且最近的CN-为12个 | |
| D. | 该晶体的一个晶胞中含有的M+的个数为4个 |
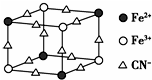
分析 根据均摊法,立方体的顶点粒子占$\frac{1}{8}$,棱上粒子占$\frac{1}{4}$,由图可推出晶体中阴离子的最小结构单元中含Fe2+个数为:4×$\frac{1}{8}$=$\frac{1}{2}$,同样可推出含Fe3+个数也为 $\frac{1}{2}$,CN-为12×$\frac{1}{4}$=3,因此阴离子为[Fe2(CN)6]-,则该晶体的化学式只能为MFe2(CN)6,由阴、阳离子形成的晶体为离子晶体,M的化合价为+1价,由图可看出与每个Fe3+距离最近且等距离的CN-为6个,图中是该晶体晶胞的八分之一,按离子的比例关系得出一个晶胞中含有的M+个数.
解答 解:A.根据均摊法,立方体的顶点粒子占$\frac{1}{8}$,棱上粒子占$\frac{1}{4}$,由图可推出晶体中阴离子的最小结构单元中含Fe2+个数为:4×$\frac{1}{8}$=$\frac{1}{2}$,同样可推出含Fe3+个数也为 $\frac{1}{2}$,CN-为12×$\frac{1}{4}$=3,因此阴离子为[Fe2(CN)6]-,则该晶体的化学式只能为MFe2(CN)6,由阴、阳离子形成的晶体为离子晶体,根据化合价代数和为零可知,M的化合价为+1价,
故A错误;
B.由A的分析可知,晶体的化学式为MFe2(CN)6,由阴、阳离子形成的晶体为离子晶体,故B错误;
C.由图可看出与每个Fe3+距离最近且等距离的CN-为6个,故C错误;
D.图中是该晶体晶胞的八分之一,其中CN-为12×$\frac{1}{4}$=3个,所以一个晶胞中的CN-有:3个÷$\frac{1}{8}$=24个,根据晶体的化学式MFe2(CN)6可知:M+与CN-的个数比为1:6,所以M+有4个,故D正确;
故选D.
点评 本题考查了用均摊法计算晶胞中原子个数的方法,如何根据原子个数确定晶体的化学式,以及判断化合价和晶体类型,判断晶体中相邻原子个数等知识点,难度适中.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:丁>丙>乙>甲 | |
| B. | 1mol A与足量B完全反应共转移了2mol电子 | |
| C. | 丙元素在周期表中的位置为第二周期第ⅣA族 | |
| D. | 甲、乙、丙、丁四种元素可以共同组成多种盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用KMnO4(H+)溶液鉴别甲苯、丙烯、已烷 | |
| B. | 用溴水鉴别苯、丙烯、四氯化碳 | |
| C. | 用水鉴别乙醇、苯、四氯化碳 | |
| D. | 用NaOH溶液鉴别溴乙烷、甲苯、硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | 深蓝色的[Cu(NH3)4]SO4溶液中加入乙醇析出晶体 | 乙醇增强了溶剂的极性 |
| B | 用KSCN检验溶液中的Fe3+ | Fe3+遇SCN-生成血红色沉淀 |
| C | CH4熔点低于CO2 | 碳氢键比碳氧键的键长短、键能大 |
| D | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题:
铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | R原子的最外层上有6个电子 | B. | RO3n-中的R只能被还原 | ||
| C. | HnRO3为强酸 | D. | R的单质既有氧化性又具有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com