
| A.反应后SO2有剩余 | B.溶液还可以吸收SO2 |
| C.溶液中除OH-外,只有一种阴离子 | D.溶液中溶质的物质的量之比为1:1 |
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:不详 题型:实验题
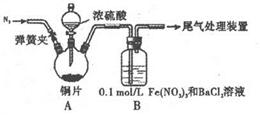
| A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称貴 |
| B.将产生的气体缓缓通入酸性髙锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀 |
| C.用排水法测定其产生气体的体积(折算成标准状况) |
| D.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.只有① | C.只有④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硫具有漂白性 | B.溴挥发而褪色 |
| C.二氧化硫具有还原性 | D.溴被还原成Br— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入铜的质量为6.4g |
| B.加入浓硫酸中溶质0.2mol |
| C.加入铜的质量大于6.4g |
| D.加入浓硫酸中含溶质多于0.2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④ | B.③④⑤ | C.①②⑤ | D.②⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
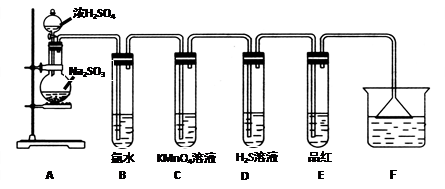
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①>②>③>④ | B.②>③>④>① |
| C.①>③>②>④ | D.③>①>②>④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
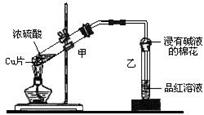
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com