
试完成下表:
| 分散系种类 | 溶液 | 胶体 | 浊液 | |||
| 水溶液 | 非水 溶液 | 粒子胶体 | 分子胶体 | 悬浊液 | 乳浊液 | |
| 分散质粒子 | 离子或分子 | 离子或分子 | 分子或离子集合体 | 大分子(高分子) | 大量分子集合的固体颗粒 | 大量分子集合的小液滴 |
| 实例 | 食盐水 | 碘酒 | Fe(OH)3胶体 | 淀粉溶液 | 石灰乳 | 牛乳 |
| 分散质粒子直径 | ||||||
| 均匀性 | ||||||
| 稳定性 | ||||||
| 能否通过滤纸 | ||||||
| 能否通过半透膜 | ||||||
| 丁达尔效应 | ||||||
科目:高中化学 来源: 题型:
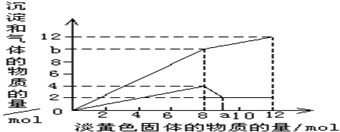 现有一种溶液,其中可能含有Mg2+、Al3+、Fe2+、Cu2+、NH4+.当加入一种淡黄色固体并加热溶解时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如图所示.试回答下列问题:
现有一种溶液,其中可能含有Mg2+、Al3+、Fe2+、Cu2+、NH4+.当加入一种淡黄色固体并加热溶解时,有刺激性气味的气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如图所示.试回答下列问题:| 可能含有的离子 (填离子符号) |
Mg2+ Mg2+ |
Al3+ Al3+ |
NH4+ NH4+ |
无 无 |
无 无 |
| 相应的物质的量 | 2mol 2mol |
2mol 2mol |
6mol 6mol |
无 无 |
无 无 |
查看答案和解析>>
科目:高中化学 来源: 题型:
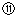 记录液面刻度的读数;
记录液面刻度的读数;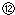 根据滴定管的两次读数得出NaOH溶液的体积为22mL
根据滴定管的两次读数得出NaOH溶液的体积为22mL| 加入NaOH溶液的体积V/mL | 0.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
| 剩余盐酸溶液的体积V/mL | 20.00 | 2.00 | 0.20 | 0.02 | 0.00 | / | / | / | / |
| 过量NaOH溶液的体积V/mL | / | / | / | / | / | 0.02 | 0.20 | 2.00 | 20.00 |
| pH | 1.00 | 2.28 | 3.30 | 7.00 | 9.70 | 11.70 | 12.50 |

查看答案和解析>>
科目:高中化学 来源: 题型:
分散系种类 | 溶液 | 胶体 | 浊液 | |||
水溶液 | 非水溶液 | 粒子胶体 | 分子胶体 | 悬浊液 | 乳浊液 | |
分散质粒子 | 离子或分子 | 离子或分子 | 分子或离子集合体 | 大分子 (高分子) | 大量分子集合的固体颗粒 | 大量分子集合的小液滴 |
实例 | 食盐水 | 碘酒 | Fe(OH)3胶体 | 淀粉溶液 | 石灰乳 | 牛乳 |
分散质粒子直径 |
|
|
| |||
均匀性 |
|
|
| |||
稳定性 |
|
|
|
| ||
能否通过滤纸 |
|
|
| |||
能否通过半透膜 |
|
|
| |||
丁达尔效应 |
|
|
| |||
查看答案和解析>>
科目:高中化学 来源: 题型:
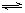 2HBr(g),已知加入1molH2和 2molBr2时,达到平衡后生成amolHBr(如下表)。在相同条件下,保持平衡时各组分的体积分数不变,试完成下表:
2HBr(g),已知加入1molH2和 2molBr2时,达到平衡后生成amolHBr(如下表)。在相同条件下,保持平衡时各组分的体积分数不变,试完成下表: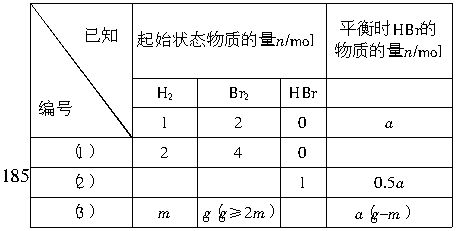
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com