
����Ŀ����֪��ӦmX��g��+nY��g��qZ��g������H��0��m+n��q���ں����ܱ������з�Ӧ�ﵽƽ��ʱ�������й�˵����ȷ���ǣ� ��
A.�������ͨ��һ����ij����ʹ��ϵѹǿ����ƽ�⽫�����ƶ�
B.��ʱ��X������Ӧ������Y���淴Ӧ���ʵ� ![]() ��
��
C.��������¶ȣ��ұ�������״̬�������ı䣬��������ƽ����Է���������С
D.�������X�����ʵ�����ƽ�������ƶ���X��ת��������
���𰸡�B
���������⣺A�����������£�ͨ��ϡ������ʹѹǿ����Ӧ������Ũ�Ȳ��䣬�����淴Ӧ���ʲ��䣬ƽ�ⲻ�ƶ�����A����B�����淴Ӧ��ƽ��ʱ��ͬ���ʱ�ʾ�������淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�X������Ӧ������Y���淴Ӧ���ʵ� ![]() ����˵����Ӧ����ƽ�⣬��B��ȷ��
����˵����Ӧ����ƽ�⣬��B��ȷ��
C�������¶�ƽ��������Ӧ�ƶ�������m+n��q����Ӧ��������ܵ����ʵ�����С������������������䣬���M= ![]() ��֪��������ƽ��Ħ���������ʽ����¶ȣ���������ƽ����Է�����������C����
��֪��������ƽ��Ħ���������ʽ����¶ȣ���������ƽ����Է�����������C����
D������X�����ʵ�����X��Ũ������ƽ�������ƶ���X��ת���ʽ��ͣ���D����
��ѡB��
�����㾫����������Ҫ�����˻�ѧƽ��״̬���ʼ����������֪ʶ�㣬��Ҫ���ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч��������ȷ�����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Ʒ��Na2CO3��NaHCO3�����Լ���ɣ���ȡ27.4g����Ʒ�����Թ��У���ּ��Ⱥ������أ������������Ϊ21.2g������
��1����Ʒ��NaHCO3������Ϊ___________g��
��2����ֽ��Ĺ����м���2mol��L��1�����ᣬʹ֮��ȫת��ΪNaCl������������������Ϊ_______L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ʯ�͵�˵������ȷ����(����)
A.ʯ����Ҫ��C��H����Ԫ��
B.ʯ��ͨ���������ɵõ���״��
C.ʯ���ѻ��������仯
D.ʯ�ͷ���õ��������ǻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ˮ�����ŷŻ����������Ⱦ�����ݳɷֲ�ͬ�ɲ��ò�ͬ�Ĵ���������
��1�����������ҵ��ˮ�г�����Cu2+���ؽ������ӣ�����FeS������������Ϊ��������ȥ����֪������Ksp��FeS��=6.3��10��18mol2L��2 �� Ksp��CuS��=1.3��10��36mol2L��2 �� ���������ӷ���ʽ˵���������ӵ�ԭ�� ��
��FeS�������ղ�����SO2����ͨ��������Һ�У��ܹ�������������������ţ�
A��Ba��NO3��2B��BaCl2
C��Ba��OH��2D������NH3��BaCl2��Һ
����֪Ԫ���ڸ�̬ʱ�����������ԣ���������CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ�����ȣ�����CuCl������������CuCl�����ӷ���ʽ�� ��
��2����ⷨ�������Ժ�����ˮ����Ҫ����Cr2O72����ʱ���ڷ�ˮ�м�������NaCl�����������������������������д������·�ӦCr2O72+6Fe2++14H+�T2Cr3++6Fe3++7H2O�����Cr3+��Cr��OH��3��ʽ��ȥ������˵������ȷ����������ţ�
A.������ӦΪFe��2e���TFe2+
B.����������ҺpH��С
C.��������Fe��OH��3��������
D.��·��ÿת��12 mol���ӣ������2mol Cr2O72������ԭ
��3���ϰ�ˮ����ת���ɰ���������Ƴɼ���ȼ�ϵ�أ�ͼ�Ǹ�ȼ�ϵ��ʾ��ͼ��������X�����ֱ���ŷŵ������У�a�缫�����������������������������������缫��ӦʽΪ �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl2��һ����Ҫ����ˮ����������������ˮ��Ӧ���ױ����������ʡ�ij��ȤС����ʵ�������Ʊ���ˮFeCl2���ⶨ�䴿�ȣ����������ʵ�飨�г�װ������ȥ��I�и�װ�ò��ظ�ʹ�ã���
��FeCl2���Ʊ�
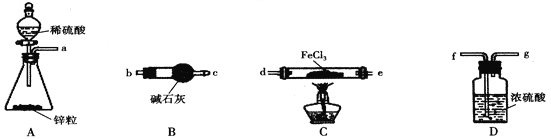
��1�����������£�H2��FeCl3�Ʊ���ˮFeCl2�Ļ�ѧ����ʽΪ______________________��
��2�������������ҵķ�����ͼ��װ�ú���������˳��Ϊ_________________���������ӿڴ�����ĸ��ʾ����
��3��װ��B������Ϊ____________��
��4����Ӧ������Ӧ��Ϩ��C���ľƾ��ƻ����ȹر�A����Һ©���Ļ���_______________���Ϩ��ƾ��ơ��رջ���������
��FeCl2�Ĵ��Ȳⶨ
��֪����ʵ��õ�����ijɷ�ΪFeCl2��FeCl3��
��Fe3����K3[Fe��CN��6]����Ӧ��3Fe2����2 [Fe��CN��6]3��![]() Fe3[Fe��CN��6]2����
Fe3[Fe��CN��6]2����
����ȤС�����������ʵ��ⶨ�õ���FeCl2��FeCl3�������FeCl2�Ĵ��ȡ�
��i����ȡm g��Ӧ��Ĺ������ڹ��������У��ٽ�������Һ��ˮϡ�͵�200 mL��
��ii��ȷ��ȡ20 mL������Һ���ձ��У����������K3[Fe��CN��6]��Һ������ɫ��Fe3[Fe��CN��6]2�������ɡ�
��iii�����ˡ�ϴ�ӡ��������г������õ�W g��ɫ���塣
��5����Ʒ��FeCl2����������Ϊ____________________________���ú���m�ͦص�ʽ�ӱ�ʾ������ͬѧ��Ϊ��������������õ�FeCl2����������ƫ�ͣ���������Ϊ______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ڵ���ʵ���
A. SO2 B. (NH4)2SO4 C. Cl2 D. NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ü�������������ȡ����Ӧ��ȡ����Ʒ����������ڹ�ҵ���ѳ�Ϊ��ʵ��ij��ѧ��ȤС��ͨ����ʵ������ģ���������̣�����Ƶ�ģ��װ�����£�

�������Ҫ��ش�
��1��Bװ�������ֹ��ܣ������������ٶȣ������Ȼ�����壻��________��
��2����V(Cl2)/V(CH4)=x��������������������Ȼ��⣬��xֵӦ________��
��3��Dװ�õ�ʯ���о��Ȼ���KI��ĩ����������________________________________________��
��4��Eװ�õ�������____________(����)��
A���ռ����� B����������
C����ֹ���� D�������Ȼ���
��5����Cװ���У�����һ��ʱ���ǿ�����䣬����Ӳ�ʲ������ڱ��к�ɫС����������д���û�����ɫС�����Ļ�ѧ����ʽ____________________________________��
��6��Eװ�ó����������⣬�������л����E�з�����л������ѷ���Ϊ________����װ�û���ȱ�ݣ�ԭ����û�н���β����������β����Ҫ�ɷ�Ϊ______(����)��
a��CH4�� b��CH3Cl ��c��CH2Cl2�� d��CHCl3 ��e��CCl4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ�����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����Ƶ���650���¹�����ȼ�ϵ�أ���֪���ط�Ӧ�൱��CO��ȼ�գ��Ҹ�����ӦʽΪ2CO+2CO ![]() ��4e��=4CO2
��4e��=4CO2
��1���õ�ص�������ӦʽΪ��
��2�����ø�ȼ�ϵ������ͼװ������ģ�ҵ���ʳ��ˮ��������Ӧ���ӵ�Դ������д����������������������ܷ�Ӧ�����ӷ���ʽΪ �� �������ͨ��0.2mol ����ʱ�����װ������������������L����״���£�����ʱ�����Һ��ֻ�ϣ���Һ��pH����������Һ����ı仯����
��3�����ø�ȼ�ϵ������Դ����NiSO4��ҺΪ�������Һ���д�������Fe��Zn��Cu��Pt��Au�����ʣ��ĵ�⾫��������˵����ȷ����������ţ�������֪�����ԣ�Fe2+��Ni2+��Cu2+��a���������У���ѧ��ת��Ϊ���� b��������������������ԭ��Ӧ
c������������ɻ���Cu��Pt��Au�Ƚ��� d����������ʱͨ���ĵ��������������������������ȣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com