

 ≡O$\stackrel{HCN}{→}$
≡O$\stackrel{HCN}{→}$ $\stackrel{H_{2}O/H+}{→}$
$\stackrel{H_{2}O/H+}{→}$
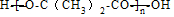 +(n-1)H2O.
+(n-1)H2O. 分析 由流程可知,CH3-CH=CH2发生加成反应生成A为CH3CHClCH3,A水解生成B为CH3CHOHCH3,B发生氧化反应生成C为(CH3)2C=O,C与HCN发生加成反应生成C为(CH3)2C(OH)CN,D水解生成E为(CH3)2C(OH)COOH,E发生缩聚反应生成G为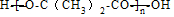 ,以此来解答.
,以此来解答.
解答 解:(1)B中所含官能团的名称是羟基,按系统命名方法可将A命名为2-氯丙烯,
故答案为:羟基;2-氯丙烯;
(2)C→D的反应类型是羰基与HCN的加成反应,故答案为:加成反应;
(3)A→B反应的化学方程式是CH3-CHCl-CH3+H2O $\stackrel{NaOH}{→}$CH3-CHOH-CH3+HCl,
故答案为:CH3-CHCl-CH3+H2O $\stackrel{NaOH}{→}$CH3-CHOH-CH3+HCl;
(4)E为(CH3)2C(OH)COOH,
a.含-OH,能发生消去反应,故正确;
b.不含碳碳双键、三键,不能使Br2/CCl4溶液褪色,故错误;
c.不含-CHO,不能发生银镜反应,故错误;
d.含-COOH,能与NaHCO3反应,故正确;
故答案为:ad;
(5)E→G反应的化学方程式是n HO-C(CH3)2-COOH$\stackrel{H_{2}SO_{4}}{→}$ 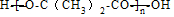 +(n-1)H2O,
+(n-1)H2O,
故答案为:n HO-C(CH3)2-COOH$\stackrel{H_{2}SO_{4}}{→}$ 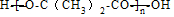 +(n-1)H2O.
+(n-1)H2O.
点评 本题考查有机物的合成,为高频考点,把握官能团的变化、碳链变化、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:推断题
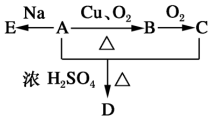 化合物A(C4H10O)是一种有机溶剂,A可以发生如图变化:
化合物A(C4H10O)是一种有机溶剂,A可以发生如图变化:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为 283 kJ | |
| B. | 反应①正反应活化能与逆反应活化能之差为+566 kJ/mol | |
| C. | 反应 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>-452 kJ/mol | |
| D. | CO(g)与 Na2O2(s)反应放出 509 kJ 热量时,电子转移数为 6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | Z |
| W | ||
| T |
| A. | W的氧化物对应水化物是强酸 | |
| B. | Z、W元素在自然界中均不能以游离态存在 | |
| C. | X、Y、Z元素的离子半径及它们的气态氢化物的热稳定性均依次递增 | |
| D. | 由元素周期律,可以推测T元素的单质具有半导体特性,T2Y3具有氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
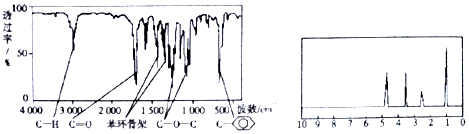
| A. | A分子属于酯类化合物,分子结构中含有酯基和苯基两种官能团 | |
| B. | A在一定条件下可与4 mol H2发生加成反应 | |
| C. | 符合题中A分子结构特征的有机物只有1种 | |
| D. | 与A属于同类化合物的同分异构体只有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
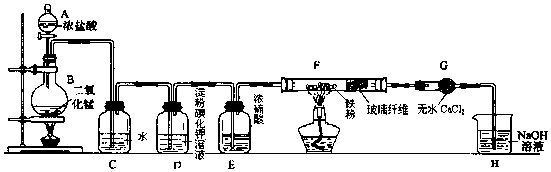
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、CH4、氟氯代烃等都会造成温窒效应,因此都属于大气污染物 | |
| B. | 测定某地区的酸雨发现经过一段时间之后pH下降,判断为硝酸型酸雨 | |
| C. | 低碳经济主要与工厂、汽车排放有关,与人们用电、用水、用纸等是否节约无关 | |
| D. | 绿色化学的核心是利用化学原理对环境污染进行治理 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com