
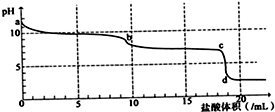
 常温下,向Na2CO3溶液中逐滴滴入0.1mol/L盐酸,溶液的pH随着滴入盐酸溶液体积变化曲线如图,则下列说法正确的是( )
常温下,向Na2CO3溶液中逐滴滴入0.1mol/L盐酸,溶液的pH随着滴入盐酸溶液体积变化曲线如图,则下列说法正确的是( )| A、a点时溶液pH=11.5,原因是:CO32-+H2O→HCO3-+OH- |
| B、a-b段发生反应为:CO32-+2H+→CO2↑+H2O |
| C、b-c段发生反应为:HCO3-+H+→CO2↑+H2O |
| D、c-d段发生反应为:H++OH-→H2O |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:

| A、负极反应为:Cu2++2e-=Cu |
| B、在外电路中,电流从负极流向正极 |
| C、电池总反应为:Zn+Cu2+=Zn2++Cu |
| D、盐桥中的阳离子移向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol钠和足量水反应可生成11.2L氢气 |
| B、常温常压下,32g氧气中含有2NA个氧分子 |
| C、1mol/LK2SO4溶液中,含有2mol钾离子 |
| D、标准状况下,22.4LHCl溶于水后溶液中含有NA个氢离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液与稀硫酸的反应 OH-+H+=H2O |
| B、氧化钙与稀盐酸反应CaO+2H+=Ca2++H2O |
| C、铁片插入硝酸银溶液中Fe+Ag+=Fe2++Ag |
| D、碳酸钙溶于稀硝酸中 CO32++2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16O与18O互为同分异构体 |
| B、16O与18O核外电子排布不同 |
| C、通过化学变化可以实现16O与18O间的转化 |
| D、标准状况下,1.12L 16O2和1.12L18O2均含有0.1NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂.草酸的盐可用作碱土金属离子的广谱沉淀剂.
草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂.草酸的盐可用作碱土金属离子的广谱沉淀剂.| 温度 | v(H2C2O4) | v(KMnO4) | KMnO4褪色时间 | |
| ①组 | 40℃ | 10ml | 10ml | 40s |
| ②组 | 40℃ | 20ml | 20ml |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com