
| A. | CH2=CHCH3分子中所有原子在一个平面上 | |
| B. | 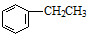 的同分异构体中,苯环上的一氯代物只有一种的结构有4种 的同分异构体中,苯环上的一氯代物只有一种的结构有4种 | |
| C. | CH2=CHCH2OH能发生加成发应、取代反应、氧化反应等 | |
| D. | 苯乙烯(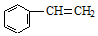 )能使溴水褪色,1mol苯乙烯与溴水反应时最多消耗4mol Br2 )能使溴水褪色,1mol苯乙烯与溴水反应时最多消耗4mol Br2 |
分析 A.含有甲基,具有甲烷的结构特点;
B.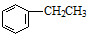 的同分异构体为二甲苯,苯环上的一氯代物只有一种,说明结构对称;
的同分异构体为二甲苯,苯环上的一氯代物只有一种,说明结构对称;
C.CH2=CHCH2OH含有羟基和碳碳双键,具有烯烃、醇的性质;
D.苯乙烯含有碳碳双键,只有碳碳双键与溴发生加成反应.
解答 解:A.含有甲基,具有甲烷的结构特点,则所有原子不可能在同一个平面上,故A错误;
B.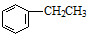 的同分异构体为二甲苯,苯环上的一氯代物只有一种,说明结构对称,应为对二甲苯,故B错误;
的同分异构体为二甲苯,苯环上的一氯代物只有一种,说明结构对称,应为对二甲苯,故B错误;
C.CH2=CHCH2OH含有羟基和碳碳双键,具有烯烃、醇的性质,可发生加成、加聚、氧化、取代和消去反应,故C正确;
D.苯乙烯含有碳碳双键,1mol苯乙烯与溴水反应时最多消耗1mol Br2,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重有机物的结构、性质以及同分异构体的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的比例模型为  ,其二氯取代物有2种结构 ,其二氯取代物有2种结构 | |
| B. | 苯和乙烯都能使溴水褪色,其褪色原理相同 | |
| C. | 相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同 | |
| D. | 在一定条件下,苯与氯气生成氯苯的反应类型是加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中一定有Fe3+,可能有Fe2+ | |
| B. | 气体通过湿润的红色石蕊试纸,试纸变蓝,证明原气体中一定含有氨气 | |
| C. | 用铂丝蘸取白色粉末灼烧,火焰成黄色,证明原粉末中一定有Na+,可能有K+ | |
| D. | 向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和浓硫酸混合加热至140℃,CH3CH2OH$→_{140℃}^{浓硫酸}$CH2=CH2↑+H2O | |
| B. | 1-溴丙烷与氢氧化钠的乙醇溶液供热:CH3CH2CH2Br+NaOH$→_{△}^{乙醇}$CH3CH2CH2OH+NaBr | |
| C. | 苯酚钠溶液中通入少量的CO2:2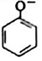 +H2O+CO2→2 +H2O+CO2→2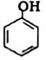 +CO${\;}_{3}^{2-}$ +CO${\;}_{3}^{2-}$ | |
| D. | 乙醛在碱性条件下被新制的氧化铜氧化:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+CuO↓+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cl-、NO3-、Fe2+ | B. | K+、Mg2+、I-、SO42- | ||
| C. | K+、Ca2+、Cl-、HCO3- | D. | Na+、Cl-、NO3-、S042- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氢氧化镍在乙醇的悬浊液中可发生如下反应生成单质镍的配合物:Ni(OH)2+5CH3NC═(CH3NC)4Ni+CH3NCO+H2O
氢氧化镍在乙醇的悬浊液中可发生如下反应生成单质镍的配合物:Ni(OH)2+5CH3NC═(CH3NC)4Ni+CH3NCO+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 该温度下此反应的平衡常数K=1.44 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正) | |
| C. | 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 | |
| D. | 0~2min的平均速率ν(Z)=2.0×10-3mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
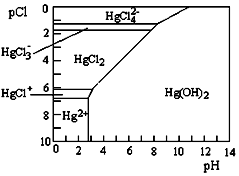 Hg是水体污染的重金属元素之一.水溶液中 二价汞的主要存在形态与Clˉ、OHˉ的浓度关系如右图所示[图中的物质或粒子只有Hg(OH)2为难溶物;pCl=-lgc(Cl-)]下列说法中不正确的是( )
Hg是水体污染的重金属元素之一.水溶液中 二价汞的主要存在形态与Clˉ、OHˉ的浓度关系如右图所示[图中的物质或粒子只有Hg(OH)2为难溶物;pCl=-lgc(Cl-)]下列说法中不正确的是( )| A. | 配制Hg(NO3)2溶液时,为了防止Hg2+水解,应将Hg(NO3)2固体溶于浓硝酸后再稀释 | |
| B. | 当c(Cl-)=0.1 mol•L-1,pH<8时,汞元素主要以HgCl3-形式存在 | |
| C. | HgCl2是一种弱电解质,其电离方程式是:2HgCl2?HgCl++HgCl3- | |
| D. | 当溶液pH保持在4,pCl由2改变至6时,可使HgCl2转化为Hg(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com