
【题目】用铝箔包装0.1mol金属钠,用针扎一些小孔,放入水中,完全反应后,用排水取气法收集产生的气体,则收集到气体的为 ( )
A. O2和H2的混合气体 B. 0.05molH2
C. 小于0.05molH2气体 D. 大于0.05molH2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)下图是在101 kPa,298K条件下1mol NO2和1mol CO反应生成1mol CO2和1mol NO过程中的能量变化示意图。
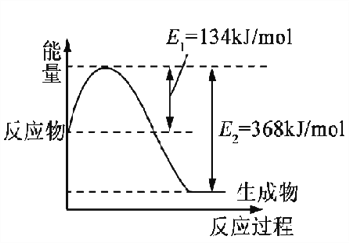
已知:① N2(g)+O2(g)=2NO(g) △H= +179.5kJ/mol
② 2NO(g)+O2(g)=2NO2(g) △H= -112.3kJ/mol
请写出NO与CO反应生成无污染气体的热化学方程式: ____________________
(2)将0.20 mol NO2和0.10 mol CO充入一个容积恒定为1L的密闭容器中发生反应,在不同条件下,反应过程中部分物质的浓度变化状况如下图所示。
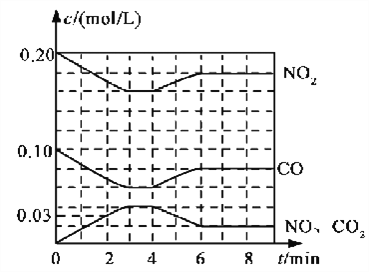
①下列说法正确的是___________(填序号)。
a.容器内的压强不发生变化说明该反应达到平衡
b.当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大
c.升高温度后,K减小,NO2的转化率减小
d.向该容器内充入He气,反应物的体积减小,浓度增大,所以反应速率增大
②计算产物NO在0~2 min内平均反应速率v(NO)=__________mol·L-1·min-1
③第4 min时改变的反应条件为__________________。
④计算反应在第6 min时的平衡常数K=________。若保持温度不变,此时再向容器中充入CO、NO各0.060 mol,平衡将________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关核酸的说法中不正确的是( )
A. 核酸是一类含磷的生物高分子化合物
B. 根据组成,核酸分为DNA和RNA
C. DNA大量存在于细胞质中
D. 1981年,我国用人工方法合成了酵母丙氨酸转移核糖核酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表示意图的一部分。
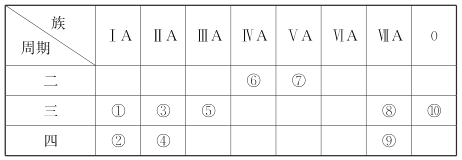
请回答下列问题:
(1)元素③~⑦中,原子半径最大的是____(填元素符号)。
(2)元素①~⑩中,最高价氧化物对应的水化物中酸性最强的是____(填化学式,下同),呈两性的氢氧化物是____。
(3)元素⑦的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置适用于实验室制氨气并验证氨气的某化学性质,其中能达到实验目的的是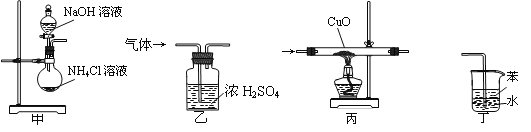
A.用装置甲制取氨气 B.用装置乙除去氨气中的水蒸气
C.用装置丙验证氨气具有还原性 D.用装置丁吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中能大量共存的是 ( )
A. 在无色溶液中: Na+ 、Fe3+、NO3- 、Cl-
B. pH=11的透明溶液中:Na+、K+、MnO4-、CO32-
C. 在含有HCO3-的溶液中:H+、K+、SO42-、Cl-
D. 含有大量Fe2+的溶液中:H+、K+、SO![]() 、NO
、NO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,回答下列问题:
主族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0族 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(1)元素①的名称是_____________;比元素⑧质子数多10的元素在周期表中所处位置___________。
(2)元素③的单质的电子式为_____________,元素③的气态氢化物与其最高价氧化物的水化物反应的化学方程式为_________________________________________。
(3)用电子式表示元素⑨与⑥的化合物的形成过程:____________________________,该化合物属于__________(填“共价或“离子”)化合物。
(4)表示②与⑦形成的化合物的电子式:________________________,该化合物是由__________(填“极性”或“非极性”)键形成的。
(5)元素⑥的氢化物的结构式为_____________________;该氢化物常温下和元素⑦的单质反应的化学方程式为________________________________;元素③④⑥形成的氢化物沸点由高到底的顺序(写化学式)___________________________。
(6)④、⑥、⑦、⑨四种元素形成的简单离子,离子半径由大到小的顺序是(写离子符号)__________________________________。
(7)某原子有6个电子、7个中子,写出其元素符号:________________________。
(8)④⑥可与氢元素构成多种10电子和18电子的粒子,其中符合下列要求的粒子的电子式为:4核18电子的分子_____________________,10电子的阳离子_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com