
| A、冰醋酸 |
| B、NaHCO3 |
| C、蔗糖 |
| D、NaOH |


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 氯水滴到蓝色石蕊试纸上 | 试纸变红色后又逐渐褪去 | 氯水中有酸性,Cl2有漂白性 |
| B | 浓硝酸滴到蓝色石蕊试纸上 | 试纸变红色后又逐渐褪去 | 浓硝酸具有酸性和强氧化性 |
| C | Fe3O4中加入足量HCl溶液,加热充分反应后,滴入KSCN溶液 | 溶液呈红色 | 盐酸将Fe3O4溶解,得到的是FeCl3溶液 |
| D | 常温下将铜、铁加入浓H2SO4 | 均不溶解 | 常温下铜、铁均不与浓H2SO4反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:Na2CO3<NaHCO3 |
| B、相同条件下,溶于水溶液的碱性:Na2CO3<NaHCO3 |
| C、常温下,在水中的溶解度:Na2CO3>NaHCO3 |
| D、相同条件下,与稀盐酸反应的快慢:Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应SiO2+3C═SiC+2CO中,氧化剂与还原剂的物质的量之比为1:2 |
| B、向蔗糖中加入浓硫酸,蔗糖变黑,并有刺激性气味,说明浓硫酸具有脱水性和强氧化性 |
| C、浓硫酸、浓硝酸在加热条件下都能将木炭氧化为二氧化碳 |
| D、铁粉与足量稀硝酸反应时,氧化剂与还原剂的物质的量之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
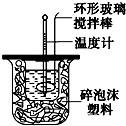 如图装置测定中和热的实验步骤如下:
如图装置测定中和热的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com