
海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
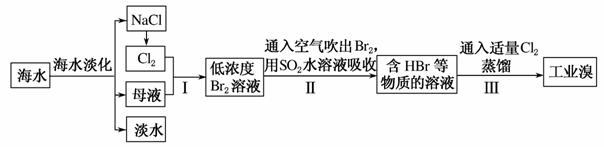
(1)请列举海水淡化的两种方法:________、________。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、________、________或H2、________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为__________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为____________________,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是________。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
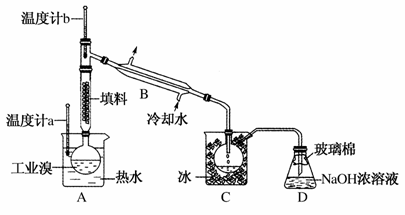
请你参与分析讨论:
①图中仪器B的名称:________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:____________________________________。
④C中液体产物颜色为________,为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行分离的操作是________。
答案 (1)蒸馏法、电渗析法、离子交换法及其他合理答案中的任意两种 (2)Cl2 NaOH NaClO (3)富集溴元素 (4)Br2+SO2+2H2O===4H++SO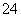 +2Br- 强酸对设备的严重腐蚀 (5)①冷凝管 ②溴腐蚀橡胶 ③控制温度计b的温度,并收集59 ℃时的馏分 ④深红棕色 分液(或蒸馏)
+2Br- 强酸对设备的严重腐蚀 (5)①冷凝管 ②溴腐蚀橡胶 ③控制温度计b的温度,并收集59 ℃时的馏分 ④深红棕色 分液(或蒸馏)
解析 (1)常规识记问题。(2)根据2NaCl+2H2O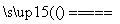 2NaOH+H2↑+Cl2↑以及Cl2+2NaOH===NaCl+NaClO+H2O可得到答案。(3)根据框图可知先前得到的溴浓度较低,这样做是使溴富集。
2NaOH+H2↑+Cl2↑以及Cl2+2NaOH===NaCl+NaClO+H2O可得到答案。(3)根据框图可知先前得到的溴浓度较低,这样做是使溴富集。
(4)Br2+SO2+2H2O===4H++SO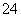 +2Br-,反应产生大量的酸,会腐蚀设备。
+2Br-,反应产生大量的酸,会腐蚀设备。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
已知X、Y是阳离子,Z是阴离子,M、N是分子,它们都由短周期元素组成,且具有
以下结构特征和性质:
①X、Y、M、N的核外电子总数相等;②常温下,M是极易溶于N的气体;③X与M均由相同的元素组成;④Y为单核离子,其与Z组成的物质可用于净水;⑤Z由同主族元素组成。请回答下列问题:
(1)X的电子式为________,Z的离子符号为________。
(2)X与Z形成的化合物中所含有的化学键类型为________。
(3)写出Y与M、N形成的混合物发生反应的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是甲、乙、丙三位同学制取乙酸乙酯的装置图,三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,请思考并回答下列问题:
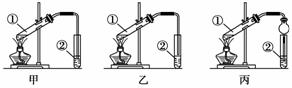
(1)请写出①中反应的化学方程式_____________________________________。
(2)甲、乙、丙三位同学设计的装置中最佳装置是________(填“甲”、“乙”或“丙”),原因是________________________________________________________________________。
(3)将3 mL乙醇、2 mL冰醋酸和2 mL浓硫酸加入试管中的先后顺序为________________________________________。浓硫酸的作用是________、________。
(4)在试管②中加入适量饱和Na2CO3溶液的作用是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.石油的分馏、煤的干馏都是物理变化
B.乙烯和聚乙烯中均含有不饱和碳碳双键
C.馒头、米饭在口腔内越嚼越甜,是因为它们含有的淀粉发生了酯化反应
D.乙醇、乙酸、乙酸乙酯都能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.使元素的化合态转化成游离态的过程就是还原的过程
B.金属冶炼的实质是金属元素被氧化
C.电解熔融氧化铝时,每还原出1 kg铝,必有111 mol电子转移
D.工业上常用电解NaCl水溶液的方法制取金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法错误的是( )
A.1 mol H2O所含电子数为10NA
B.1 mol Al与足量的稀盐酸溶液反应生成氢气1.5 mol
C.在标准状况下,0.5NA Cl2所占的体积约是11.2 L
D.在非标准状况下,22.4 L O2含有的分子数一定不是NA
查看答案和解析>>
科目:高中化学 来源: 题型:
关于1 mol·L-1的硫酸溶液,下列叙述中不正确的是( )
A.1 L该溶液中含溶质98 g
B.从10 mL该溶液中取出5 mL后,剩余溶液的浓度为1 mol·L-1
C.将4.9 g浓硫酸加入盛有50 mL蒸馏水的烧杯中,充分溶解后就可配得该浓度的硫酸溶液
D.该浓度的硫酸具有酸的通性,可与锌反应制取氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列陈述Ⅰ、Ⅱ均正确且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Fe3+有氧化性 | FeCl3溶液可溶解废旧电路板中的铜 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | NH3有还原性 | NH3可用H2SO4吸收 |
| D | 浓HNO3有酸性 | 浓HNO3不可用铁制容器盛放 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
用石灰水保存鲜蛋是一种化学保鲜法,石灰水能保存鲜蛋的原理是( )
①石灰水具有强碱性,杀菌能力强
②Ca(OH)2能与鲜蛋呼出的CO2反应,生成CaCO3薄膜,起保护作用
③石灰水是电解质溶液,能使蛋白质凝聚
④石灰水能渗入蛋内中和酸性物质
A.①② B.③④
C.②④ D.①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com