
��һ���¶��£���2.0�����N����6.0�����H��ͨ��һ��������������ɱ�������У�������һ���������ͨ�������з������·�Ӧ��������������![]() ���Σ�����
��������
��֪ƽ��ʱ�Σ�����Ũ����c mol��L�������ְ��������������Ϊ��ʼ���ʣ��ֱ���������������������¶Ȳ��䣬��ﵽƽ���NH����Ũ�Ȳ�Ϊc mol��L�������ǣ� ��
A.1.0�����N����3.0�����H��
B.2.0�����N����6.0�����H����4.0�����NH��
C.4.0�����NH����1.0�����H��
D.2.0�����NH��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
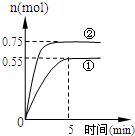 ̼ѭ����;��֮һ�ǣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g��+49.0kJ�����ݻ�Ϊ2L���ܱ������г���1mol CO2��3mol H2�������ֲ�ͬ��ʵ�������½��з�Ӧ�����CH3OH��g�������ʵ�����ʱ��仯�������ͼ��ʾ��
̼ѭ����;��֮һ�ǣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g��+49.0kJ�����ݻ�Ϊ2L���ܱ������г���1mol CO2��3mol H2�������ֲ�ͬ��ʵ�������½��з�Ӧ�����CH3OH��g�������ʵ�����ʱ��仯�������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����a=0��b=0����c=______________��
��2����a=0.5����b=_______________��c=______________��
��3��a��b��c���������һ�������ǣ�������������ʽ��ʾ������һ��ֻ��a��c����һ��ֻ��b��c����_________________��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£���2 mol SO2��1mol O2ͨ��һ��һ���ݻ����ܱ�������������·�Ӧ��
����2SO2(g)+O2(g) ![]() 2SO3(g)
2SO3(g)
�������˷�Ӧ���е�һ���̶�ʱ����Ӧ�����ʹ���ƽ��״̬�����ڸ�������ά���¶Ȳ��䣬��a��b��c�ֱ������ʼ�����SO2��O2��SO3�����ʵ��������a��b��cȡ��ͬ����ֵ�����DZ�������һ�������ϵ�����ܱ�֤ƽ��ʱ��Ӧ�������3������İٷֺ������Ը�����ƽ��ʱ��ȫ��ͬ������д���пհף�
������1����a=0,b=0,��c��___________��
������2����a=0.5,��b��___________��c=___________��
������3��a��b��cȡֵ���������һ�������ǣ�������������ʽ��ʾ������һ��ֻ��a��c����һ��ֻ��b��c����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���¶��£���2.0���N2��6.0���H2ͨ��һ��������������ɱ�������У�������һ���������ͨ����ͼ��ʾ�������з����ķ�Ӧ���£�
![]() N2��3H2 2NH3������Ӧ���ȣ�
N2��3H2 2NH3������Ӧ���ȣ�

����Ӧ�ﵽƽ���û������Ϊ7.0������Իش�
��1������������Ӧ�¶Ȳ��䣬��a��b��c(a��b=1��3)�ֱ������ʼ�����N2��H2��NH3������������Ӧ�ﵽƽ���������и����ʵ����������������ƽ����ȫ��ͬ����ô��
����a=1.0��c=2.0����b=___________���ڴ�����£���Ӧ��ʼʱ����___________������У���������棩��
�����涨��ʼʱ��Ӧ���淽����У���c�ķ�Χ��_______�����ú�a��b��ʽ�ӱ�ʾ����
��2��������װ���У��������ƽ���������Ϊ6.5�������ɲ�ȡ�Ĵ�ʩ��______
ԭ����___________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com