
| A、一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度 |
| B、常温下,向Mg(OH)2饱和溶液中加入NaOH溶液,Mg(OH)2的Ksp不变 |
| C、带有“盐桥”的铜锌原电池比不带“盐桥”的铜锌原电池电流持续时间长 |
| D、对滴加酚酞的NaHCO3溶液加热,红色加深,是因为加热时NaHCO3分解生成Na2CO3,碱性增强 |


科目:高中化学 来源: 题型:
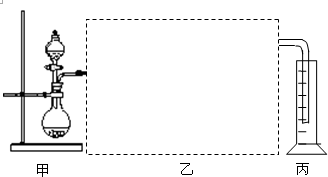
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
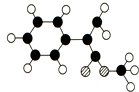
 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
 T℃时,容积固定为1L的密闭容器甲中充入2molSO2、1molO2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,维持温度为T℃,4min后达到平衡,测得平衡时n(SO3)=1.2mol.
T℃时,容积固定为1L的密闭容器甲中充入2molSO2、1molO2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,维持温度为T℃,4min后达到平衡,测得平衡时n(SO3)=1.2mol.查看答案和解析>>
科目:高中化学 来源: 题型:
| 条件变化 | c(CH3COO-) | c(H+) | 平衡移动方向 |
| 加少量HCl | |||
| 加CH3COONa固体 | |||
| 加少量NaOH固体 | |||
| 加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离的c(H+):①=②=③=④ |
| B、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| C、将②、③溶液混合后,若pH=7,则消耗溶液的体积:②>③ |
| D、四种溶液均稀释100倍后,溶液的pH:③>④>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a>b | B、a<b |
| C、a=b | D、不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三个烧杯中一定均会发生的离子反应有:2Na+2H2O═2Na++2OH-+H2↑ |
| B、三个烧杯中钠均在液面上剧烈反应,相比而言,X烧杯中的反应平缓些 |
| C、Z烧杯中一定会有沉淀生成,但沉淀不是单质铜 |
| D、三个烧杯中生成氢气体的物质的量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com