
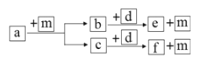
【题目】短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d为淡黄色的离子化合物,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法正确的是
A. 原子半径: W<X<Y<Z
B. 阴离子的还原性: Y>W
C. 图中物质的转化过程均为氧化还原反应
D. a 一定由 W、X 两种元素组成
【答案】C
【解析】短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d 是淡黄色粉末,d为Na2O2,m 为元素 Y 的单质,通常为无色无味的气体m为O2,则Y为O,a为烃,b、c分别为CO2、H2O,e、f分别为NaOH、碳酸钠,结合原子序数可知,W为H,X为C,Y为O,Z为Na,以此解答该题。
由上述分析可知,W为H,X为C,Y为O,Z为Na,A.同周期元素从左到右原子半径逐渐减小,应为C>O,选项A错误;B.由NaH+H2O=NaOH+H2↑,可知H-失去电子,阴离子的还原性:Y<W,选项B错误;C.题中物质的转化都涉及氧气的参与,一定为氧化还原反应,选项C正确;D.a燃烧生成水、二氧化碳,可为烃或烃的含氧衍生物,选项D错误。答案选C。


科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在体积为2 L的密闭容器中混合,并在一定条件下发生反应:2A(g)+B(g)![]() xC(g),若经2s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6mol/L。现有下列几种说法:①2s内用物质A表示的平均反应速率为0.3 mol/(L·s);②2s内用物质B表示的平均反应速率为0.6 mol/(L·s);③2s时物质B的转化率为70%;④x=2。其中正确的是( )
xC(g),若经2s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6mol/L。现有下列几种说法:①2s内用物质A表示的平均反应速率为0.3 mol/(L·s);②2s内用物质B表示的平均反应速率为0.6 mol/(L·s);③2s时物质B的转化率为70%;④x=2。其中正确的是( )
A. ①③ B. ②③ C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于离子键、共价键的各种叙述中,下列说法中正确的是
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如 Cl2)中
C.原子序数为 11 与 9 的元素能够形成离子化合物,该化合物中存在离子键
D.任何物质中都存在化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA为阿伏加德罗常数的数值.下列说法正确的是
A. 标准状况下, 78g 苯中含有碳碳双键的数目是 3 NA
B. 18g D2O 含有 10NA个质子
C. 28 g 聚乙烯中含有的原子数目为 6NA
D. 56g 铁片投入足量浓 H2SO4中生成 NA个 SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
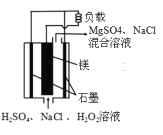
【题目】镁-过氧化氢燃料电池具有比能量高。安全方便等优点。其结构示意图如图所示、关于该电池的叙述正确的是
A. 该电池能在高温下正常工作
B. 电流工作时, H+向 Mg 电极移动
C. 电池工作时,正极周围溶液的pH将不断变小
D. 该电池的总反应式为: 该电池的总反应式为Mg+H2O2+H2SO4=MgSO4+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
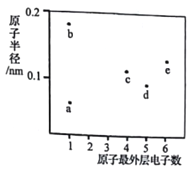
【题目】a、b、c、d、e五种短周期元素的原子半径和最外层电子数之间的关系如图所示:下列说法正确的是
A. 离子半径:b>d
B. 沸点:a与d形成的化合物>a与c形成的化合物
C. a与b、c、d、e均可形成共价化合物
D. e的含氧酸可能既有氧化性又有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.4mol CuSO4和0.4mol NaCl溶于水,配成1L溶液,用惰性电极进行电解,当一个电极得到0.3mol Cu时,另一个电极上生成的气体在标准状况下的体积是( )
A.5.6L
B.6.72L
C.1.344L
D.11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于SO2的叙述正确的是( )
A.SO2是无色无味有毒的气体B.SO2有毒,不能做食品添加剂
C.SO2不溶于水D.SO2与NaOH反应能生成Na2SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。
查阅资料:①实验室用饱和NaNO2与NH4Cl溶液共热制N2:NaNO2+NH4Cl![]() NaCl+N2↑+2H2O。
NaCl+N2↑+2H2O。
②工业制氮化铝:Al2O3+3C+N2![]() 2AlN+3CO,氮化铝在高温下能水解。
2AlN+3CO,氮化铝在高温下能水解。
③AlN与NaOH饱和溶液反应:AlN+NaOH+H2O![]() NaAlO2+NH3↑。
NaAlO2+NH3↑。
Ⅰ.氮化铝的制备
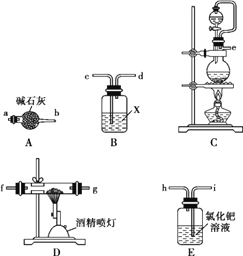
(1)实验中使用的装置如上图所示,请按照氮气气流方向将各仪器接口连接:e→c→d→____________(根据实验需要,上述装置可使用多次)。
(2)B装置内的X液体可能是____;E装置内氯化钯溶液的作用可能是_______。
Ⅱ.氮化铝纯度的测定
【方案ⅰ】甲同学用下图装置测定AlN的纯度(部分夹持装置已略去)。
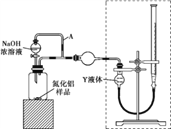
(3)为准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是____。
a.CCl4 b.H2O c.NH4Cl饱和溶液 d.植物油
(4)若装置中分液漏斗与导气管之间没有导管A连通,对所测AlN纯度的影响是____ (填“偏大”“偏小”或“不变”)。
【方案ⅱ】乙同学按以下步骤测定样品中AlN的纯度。
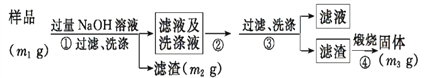
(5)步骤②的操作是_________。
(6)实验室里煅烧滤渣使其分解,除了必要的热源和三脚架以外,还需要的仪器有______等。
(7) 样品中AlN的纯度是__________(用m1、m2、m3表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com