
| A. | Cl-→Cl2 | B. | I2→I- | C. | Fe3+→Fe2+ | D. | CO32-→CO2 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
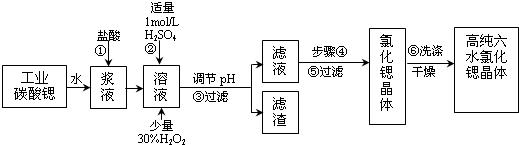
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粉尘较多的环境--易患(诱发)肺病 | |
| B. | NO2和SO2排入大气中--导致酸雨 | |
| C. | 汽车尾气(含氮的氧化物等)--造成光化学烟雾 | |
| D. | 滥用化肥及含磷洗衣粉--重金属元素污染水土 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 密度 | B. | 原子数 | C. | 质量 | D. | 分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ | B. | Fe3+ | C. | Cl- | D. | Fe2+ | ||||
| E. | Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 | |
| B. | 乙烷和丙烯的物质的量共1 mol,完全燃烧生成3 mol H2O | |
| C. | 用水可区分苯和溴苯 | |
| D. | 结构如图(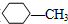 )的物质其一氯代物有4种 )的物质其一氯代物有4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com