

���� ̼������Ʒ����ˮ�����뱥��ʯ��ˮ������̼��Ƴ��������˵�����Ϊ̼��ƣ���Һ�к����������ơ��Ȼ��Ƶȣ���̼���ϴ�ӡ����������㣬����̼��Ƶ������ɼ���̼���Ƶ����������ݴ˼���̼���Ƶ�����������
��1�����˿ɳ�ȥ�����Թ������ʣ������ݹ������������������
��2��̼���ƺ��������Ʒ�Ӧ����̼��Ƴ������������ƣ������Ԫ���غ�͵���غ���д���ӷ���ʽ��
��3����������ķ�����Һ�м�ϡ���ᣬ���������ݲ���������̼̼���ƣ�������������Һ�к���̼���ƣ�˵��ʯ��ˮ��������̼���Ƴ�������ȫ���ݴ��жϣ�
��4����������ķ�����֪���μ�����ǰ��Һ�е����ʳ��Ȼ����⣬һ���������������ƣ����Եμ����ᷢ���кͷ�Ӧ���ݴ˴��⣮
��� �⣺��1������A�������Һ����룬�������ù��˵ķ��������˹������õ��IJ����������ձ���©������������
�ʴ�Ϊ��©������������
��2����Ʒ�е��Ȼ������������Ʋ���Ӧ��̼���ƺ��������Ʒ�Ӧ����̼��Ƴ������������ƣ���Ӧ�����ӷ���ʽ��CO32-+Ca2+�TCaCO3����
�ʴ�Ϊ��CO32-+Ca2+�TCaCO3����
��3����������ķ�����Һ�м�ϡ���ᣬ���������ݲ���������̼̼���ƣ�������������Һ�к���̼���ƣ�˵��ʯ��ˮ��������̼���Ƴ�������ȫ���ݴ˼��������̼���Ƶ���������ƫС��
�ʴ�Ϊ��Na2CO3��ƫС��
��4����������ķ�����֪���μ�����ǰ��Һ�е����ʳ��Ȼ����⣬һ���������������ƣ����Եμ����ᷢ���кͷ�Ӧ����Ӧ�����ӷ���ʽΪOH-+H+�TH2O��
�ʴ�Ϊ��NaOH��OH-+H+�TH2O��
���� ���⿼����ѧ�������ͽ���������������ȷÿһ�������ú��������Ļ�ѧ��Ӧ������ȷ����Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʯ���Ժ�ɫ | B�� | ʳ�û������ܷ���ˮ�ⷴӦ | ||
| C�� | ��װ�ò��Ͼ�����ϩ������ | D�� | PX��Ŀ�еĶԶ��ױ����ڱ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
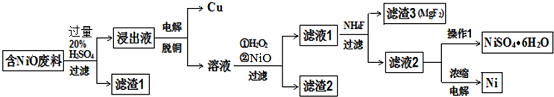
| ���� | Fe��OH��3 | Al��OH��3 | Ni��OH��2 | Fe��OH��2 | Mg��OH��2 |
| ��ʼ���� | 1.5 | 3.6 | 7.3 | 7.0 | 9.6 |
| ��ȫ���� | 3.8 | 4.7 | 9.3 | 9.0 | 12.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ�� Ũ�� ���� | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol•L-1 | 0.13mol•L-1 | 0.1mol•L-1 | 0.1mol•L-1 | 0.09mol•L-1 |
| H2 | 0mol•L-1 | 0.2mol•L-1 | 0.3mol•L-1 | 0.3mol•L-1 | 0.33mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �����K��N���ӣ������������ḯʴ | |
| B�� | �����K��N���ӣ�������Ӧʽ��4OH--4e-�T2H2O+O2�� | |
| C�� | �����K��M���ӣ���ʯī������ͭ������ʵ�������϶�ͭ | |
| D�� | �����K��M���ӣ�������������22.4L����״��������ʱ��������1mol NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����һ��������С��Ԫ����Cu����Ԫ�ط��ţ���
����һ��������С��Ԫ����Cu����Ԫ�ط��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƾ���ʹ�����ʱ��ԣ�ҽѧ��ʹ����ˮ�ƾ���ɱ������ | |
| B�� | NH3����ˮ���Լ��ԣ���FeCl3������Һ��ͨ������NH3����ȡFe��OH��3���� | |
| C�� | ClO2����ǿ�����ԣ�����������ˮ��ɱ�������������������ĸ�Ч��ȫ�� | |
| D�� | Na2CO3�������ᷴӦ���㷺��������θ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com