
分析 (1)依据配制溶液体积选择合适规格容量瓶;
(2)依据C=$\frac{1000ωρ}{M}$计算浓盐酸的物质的量浓度,依据溶液稀释过程中溶质的物质的量不变计算需要浓盐酸的体积;根据“大而近”的原则,根据需要量取的浓盐酸的体积来选择合适的量筒;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
(5)液体试剂应保存在细口瓶中.
解答 解:(1)配制220mL溶液,实验室没有220mL容量瓶,所以应选择250mL容量瓶;
故答案为:250;
(2)质量分数为37.5%的浓盐酸(密度为1.16g/cm3)物质的量浓度为$\frac{1000×1.16×37.5%}{36.5}$=11.9mol/L,设需要浓盐酸体积为V,则依据溶液稀释过程中溶质的物质的量浓度不变得:11.9mol/L×V=1mol/L×250mL,解得V=21.0mL;根据“大而近”的原则,根据需要量取的浓盐酸的体积为21.0mL来选择合适的量筒,故应选择25mL量筒,
故答案为:21.0;C;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序可有:③①④②;
故答案为:③①④②;
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,导致量取的盐酸中含有氯化氢物质的量偏小,其配制的稀盐酸浓度偏低;若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,导致部分溶质损耗,溶质的物质的量偏小,则配制的稀盐酸浓度偏低;
故答案为:偏低;偏低;
(5)配制完后,应将容量瓶中的稀盐酸转移到细口的试剂瓶中存放,盖好塞子并贴上标签;
故答案为:细口.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,明确配制原理及操作步骤是解题关键,难度不大.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 通人过量氯气:Fe2+、NH4+、H+、SO42-、Cl- | |
| B. | 加入少量 NaClO溶液:Fe2+、NH4+、SO42-、H+、ClO | |
| C. | 加入过量 NaOH 溶液:Na+、Fe2+、NH4+、SO42-、OH- | |
| D. | 加入过量NaClO和NaOH的混合溶液:Na+、SO42-、Cl-、ClO-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 | 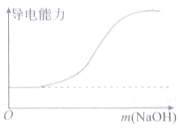 |
| A.向100mL 0.1mol•L-1H2SO4溶液中滴加 0.1mol•L-1Ba(OH)2溶液至过量 | B.向100mL 0.1mol•L-1H2SO4溶液中加入NaOH固体 |
 |  |
| C.向一定浓度的氯化钠溶液中加水 | D.向蒸馏水中通入HCl气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正常雨水pH等于7,酸雨的PH小于7 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| C. | 铝比铁活泼,所以铝比铁更容易被腐蚀 | |
| D. | CO2通入可溶性硅酸盐中析出硅酸沉淀,所以硅酸的酸性小于碳酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大力发展电动车,减少燃油汽车的尾气排放量 | |
| B. | 开发利用各种新能源,减少对化石燃料的依赖 | |
| C. | PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 | |
| D. | 多环芳烃是强致癌物,能吸附在PM2.5的表面进入人体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
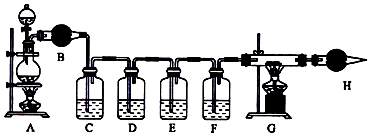
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若混合后溶液中c(H+)>c(OH-),则一定有V1<V2 | |
| B. | 若V1=V2,则二者混合后的溶液中pH>7 | |
| C. | 混合溶液中可能存在:c ( F-)>c (H+)>c (Na+)>c( OH-) | |
| D. | 二者恰好反应完时,则所得溶液中c(F-)=c (Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀盐酸反应 | B. | 灼热的炭与水蒸气的反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 甲烷在氧气中的燃烧反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com