
清洗和制绒是硅晶片制作的重要步骤之一,硅片化学清洗的主要目的是除去硅片表面杂质(如某些有机物,无机盐,金属、Si、SiO2粉尘等)。常用的化学清洗剂有高纯水、有机溶剂、双氧水、浓酸、强碱等。其中去除硅的氧化物,通常用一定浓度的HF溶液,室温条件下将硅片浸泡1至数分钟。制绒是在硅片表面形成金字塔形的绒面,增加硅对太阳光的吸收。单晶制绒通常用NaOH,Na2SiO3等混合溶液在75~90℃反应25~35 min,效果良好。
回答下列问题
(1)能否用玻璃试剂瓶来盛HF溶液,为什么?用化学方程式加以解释 ;
(2)写出晶片制绒反应的离子方程式 ,对单晶制绒1990年化学家Seidel提出了一种的电化学模型,他指出Si与NaOH溶液的反应,首先是Si与OH一反应,生成SiO44一,然后SiO44一迅速水解生成H4SiO4。基于此原理分析反应中氧化剂为 。
(3)本校化学兴趣小组同学,为验证Seidel的理论是否正确,完成以下实验:
| | 实验事实 |
| 事实一 | 水蒸汽在600℃时可使粉末状硅缓慢氧化并放出氢气。 |
| 事实二 | 盛放于铂或石英器皿中的纯水长时间对粉末状还原硅无腐蚀作用。 |
| 事实三 | 普通玻璃器皿中的水仅因含有从玻璃中溶出的微量的碱便可使粉末状硅在其中缓慢溶解。 |
| 事实四 | 在野外环境里,用较高百分比的硅铁粉与干燥的Ca(OH)2和NaOH,点着后焖烧,可剧烈放出H2。 |
| 事实五 | 1g(0.036mo1)Si和20mL含有lgNaOH(0.025mol)的溶液,小心加热(稍微预热),收集到约1700mL H2,很接近理论值(1600mL)。 |
(10分,除标记外,其余每空2分)(1)SiO2+4HF=SiF4↑+2H2O
(2)Si+2OH一+H2O=SiO32-+2H2↑;NaOH;
(3)氧化 催化 活化能 氧化(每空各1分) (4)C
解析试题分析:(1)因为氢氟酸能和二氧化硅反应,从而腐蚀玻璃,反应的化学方程式为SiO2+4HF=SiF4↑+2H2O,因此不能用玻璃试剂瓶来盛HF溶液。
(2)硅单质能和氢氧化钠溶液反应生成硅酸钠和氢气,所以晶片制绒反应的离子方程式为Si+2OH一+H2O=SiO32-+2H2↑;Si与OH一反应,生成SiO44一,这说明在反应中氧化剂应该是氢氧化钠。
(3)水蒸汽在600℃时可使粉末状硅缓慢氧化并放出氢气,而普通玻璃器皿中的水仅因含有从玻璃中溶出的微量的碱便可使粉末状硅在其中,这说明在碱性水溶液条件下,H2O可作氧化剂。少量的氢氧化钠可以加快反应速率,这说明氢氧化钠通过降低反应的活化能,起催化剂的作用。在野外环境里,用较高百分比的硅铁粉与干燥的Ca(OH)2和NaOH,点着后焖烧,可剧烈放出H2,这说明在高温无水环境下,NaOH起氧化剂的作用,与硅反应放出氢气。
(4)A、硅烷在常温下与空气和水剧烈反应,因此在使用硅烷时要注意隔离空气和水,这是由于SiH4能与水发生氧化还原反应生成H2,A正确;B、在反应3SiH4+4NH3=Si3N4+12H2↑中,氨气中氢元素的化合价从+1价降低到0价得到电子,所以反应中NH3作氧化剂,硅烷是还原剂,B正确;C、氮化硅的性质稳定,但硅烷的性质很活泼,常温下与空气和水剧烈反应,因此选项C不正确;D、氮和硅都是非金属,因此氮化硅晶体中只存在共价键,Si3N4是优良的新型无机非金属材料,D正确,答案选C。
考点:考查硅及其化合物的结构、性质、用途以及实验方案设计与评价等


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:填空题
硅在地壳中的含量较高,硅及其化合物的开发由来已久,在现代生活中有广泛应用。回答下列问题:
(1)陶瓷、水泥和玻璃是常用的传统的无机非金属材料,其中生产普通玻璃的主要原料有 。
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下: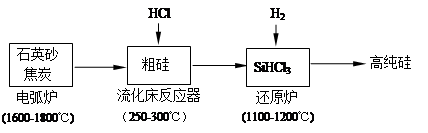
①工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃除生成粗硅外,也可以生产碳化硅,则在电弧炉内可能发生的反应的化学方程式为 。
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应方程式 。
(3)有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和 ;SiHCl3极易水解,其完全水解的产物为 。
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图是现今常规生产发烟硫酸和硫酸的流程图: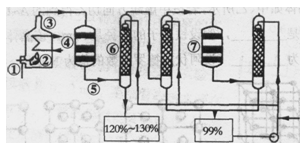
(1)在④处二氧化硫被氧化成三氧化硫,④的设备名称是 .该处发生反应的方程式为 .为提高三氧化硫的产率,该处应采用 (填“等温过程”或“绝热过程”)为宜.
(2)在⑦处进行二次催化处理的原因是 .
(3)⑤处气体混合物主要是氮气和三氧化硫.此时气体经过⑥后不立即进入⑦是因为: .
(4)20%的发烟硫酸(SO3的质量分数为20%)1吨需加水 吨(保留2位有效数字)才能配制成98%的成品硫酸.
(5)在②处发生1500℃的“不完全燃烧”,即先混入少量干燥空气,然后在③处于700℃下再继续燃烧.试简述这种燃烧方式对环境保护是有利的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
金刚石SiC具有优良的耐磨、耐腐蚀特性,应用广泛.
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物H为非极性分子,碳元素在周期表中的位置是,Q是,R的电子式为.
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为,除去粗产品中少量钠的试剂为.
(3)碳还原制SiC,其粗产品中杂质为Si和SiO2.先将20.0g 粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L,生成氢气的离子方程式为,硅酸钠的物质的量浓度为
粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L,生成氢气的离子方程式为,硅酸钠的物质的量浓度为
(4)下列叙述正确的有(填序号),ks5u
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应②水晶、干冰熔化时克服粒子间作用力的类型相同③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氨和联氨(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。根据
题意完成下列计算:
联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮
原子的质量分数为0.977,计算确定该氢化物的分子式为 。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积 L。
联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物
是氮气和水。由联氨和四氧化二氮组成的火箭推进剂恰好完全反应生成72.0 kg水,推进剂中联氨的质量为 kg。
氨的水溶液可用于吸收NO与NO2混合气体,可消除氮氧化合物对环境的污染。请分
别写出有关的反应方程式为: ; 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中。在人体的很多生理过程中也起着重要作用。
| 资料:① H2S可溶于水(约1:2),其水溶液为二元弱酸。 ② H2S可与许多金属离子反应生成沉淀。 ③ H2S在空气中燃烧,火焰呈淡蓝色。 |
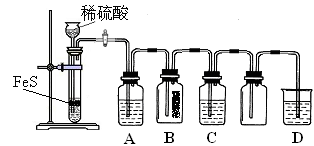
| | 实验操作 | 实验现象 |
| 实验1 | 将等浓度的Na2S和Na2SO3溶液按体积比2∶1混合 | 无明显现象 |
| 实验2 | 将H2S通入Na2SO3溶液中 | 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 | 将SO2通入Na2S溶液中 | 有浅黄色沉淀产生 |
 |  |  |  |
| A | B | C | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示为A、B、C、D、E五种含氮物质相互转化的关系图,其中A、B、C、D常温下都是气体,B为红棕色,写出各步反应的化学方程式。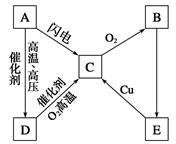
A→C:______________________________________,
D→C:_______________________________________,
B→E:_______________________________________,
E→C:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
化学肥料在农业生产中有重要作用。农业生产中,大量施用的化肥主要是氮肥、磷肥、钾肥。
(1)普钙是磷肥,它的有效成分是__________________(写化学式)。
(2)尿素是一种含氮量较高的氮肥,工业生产尿素是将氨气与二氧化碳在加压、加热的条件下反应生成氨基甲酸铵(H2NCOONH4),再使氨基甲酸铵脱水得到尿素。反应的化学方程式为_________、___________。
(3)某化肥厂用NH3制备NH4NO3,已知由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去NH3的质量占耗用全部NH3质量的__________%。
(4)合成氨气是生产氮肥的重要环节。合成氨生产简易流程示意图如下: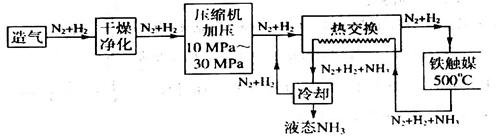
从示意图可知其存在循环操作。简要说明为什么在化工生产中经常采用循环操作___________。合成氨的反应需在500℃进行,其主要原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置: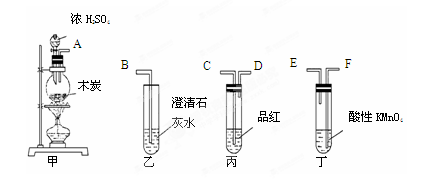
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
接 , 接 , 接 ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?
乙中 ____ ,丙中 ______ ;
(3)丁中酸性KMnO4溶液的作用是 ;
(4)写出甲中反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com