
【题目】元素周期表短周期的一部分如图所示.下列有关A,B,C,D,E五种元素的叙述中,正确的是( ) 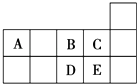
A.D在过量的B中燃烧的主要产物为DB3
B.C的氢化物的水溶液酸性比E的强
C.A与B形成的阴离子可能有AB32﹣、A2B42﹣
D.原子半径:A>B>C
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等.实验室可用工业碳酸钙(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙,其主要流程如下: 
已知:CaO28H2O呈白色微溶于水,加热至350℃左右开始分解放出氧气,425℃分解完全.
(1)写出反应①中氧化还原反应的离子方程式: .
(2)向反应①后的溶液中加浓氨水的目的是: , (用方程式表示)
(3)反应②常用冰水控制温度在0℃左右,其可能原因是(写出两种):①;② .
(4)测定产品中CaO2的含量的实验步骤是
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的H2SO4溶液,充分反应.
第二步:向上述锥形瓶中加入几滴淀粉溶液.
第三步:逐滴加入浓度为c molL﹣1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL.已知:I2+2S2O32﹣═2I﹣+S4O62﹣ .
某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能(填“不受影响”“偏低”或“偏高”),原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,4L密闭容器内某一反应中气体M,气体N的物质的量随时间变化的曲线如图所示: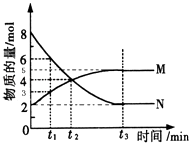
(1)比较t2时刻,正逆反应速率大小v正 v逆 . (填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻,M的平均化学反应速率为:
(3)t3时刻化学反应达到平衡时反应物的转化率为
(4)如果升高温度则v逆(填增大、减小或不变).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在水溶液中的电离方程式正确的是( )
A.NaHSO4═Na++HSO ![]()
B.Al2(SO4)3═2Al3++3SO ![]()
C.NH4Cl═NH3+H++Cl﹣
D.H2CO3═2H++CO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分: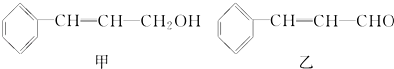
丙(见下表)
分子式 | C16H14O2 |
部分性质 | 能使Br2/CCl4褪色 |
能在稀H2SO4中水解 |
(1)甲的分子式为:
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):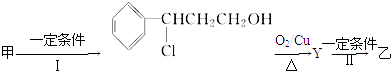
反应Ⅱ的化学方程式为(注明反应条件).
(3)已知:RCH═ CHR′ ![]() RCHO+R′CHO;2CHO
RCHO+R′CHO;2CHO ![]() HCOOH+CH3OH
HCOOH+CH3OH
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):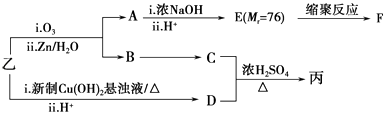
①下列物质不能与C反应的是(选填序号).
a.金属钠 b.乙酸 c.Na2CO3溶液 d. HBr
②写出F的结构简式 .
③D有多种同分异构体,任写其中一种能同时满足下列条件的异构体的结构简式 .
a.苯环上连接三种不同官能团 b.能发生银镜反应
c.能与Br2/CCl4发生加成反应 d.遇FeCl3溶液显示特征颜色
④综上分析,丙的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学要配制85mL 0.1molL﹣1 Na2CO3溶液.下图是一些关键步骤和操作.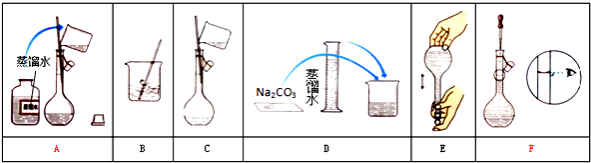
(1)配制过程的先后顺序为(用字母A~F填写) .
(2)配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、、 .
(3)容量瓶上需标有:①温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式或碱式
A.①③⑤
B.③⑤⑥
C.①②④
D.②④⑥
(4)若用Na2CO310H2O晶体来配制溶液,需用托盘天平称量固体 .
(5)在步骤B之后,需才进行下一步操作.
(6)下列操作使配得的溶液浓度偏低的是①Na2CO310H2O晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠 ④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶用蒸馏水洗涤后未经干燥就使用 ⑥转移过程中没有洗涤烧杯
⑦定容时仰视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:X(g)+2Y(g) ![]() 3Z(g) ΔH=-a kJ·molˉ1(a>0)。下列说法不正确的是( )
3Z(g) ΔH=-a kJ·molˉ1(a>0)。下列说法不正确的是( )
A.0.1 mol X和0.2 mol Y充分反应生成Z的物质的量一定小于0.3 mol
B.达到化学平衡状态时,X、Y、Z的浓度不再发生变化
C.达到化学平衡状态时,反应放出的总热量可达a kJ
D.升高反应温度,逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)为除去CuSO4溶液中少量的Fe3+杂质,可加入某物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3而除去,调整溶液pH可选用下列物质中的________。
A. NaOH B. Cu C. Cu(OH)2 D. NH3·H2O
(2)在恒温、恒容条件下,将1molA和2molB充入一个密闭容器中,在一定条件下发生反应:A(g)+2B(g)![]() xC(g),达到平衡时,测得C的物质的量分数为m%;若开始充入容器中的是0.3mol A、0.6mol B和1.4mol C,达平衡时C的物质的量分数仍为m%,则x的值为_________________ 。
xC(g),达到平衡时,测得C的物质的量分数为m%;若开始充入容器中的是0.3mol A、0.6mol B和1.4mol C,达平衡时C的物质的量分数仍为m%,则x的值为_________________ 。
(3)25℃时,物质的量浓度相同的下列六种溶液:①NH3·H2O ②NH4HSO4 ③(NH4)2CO3 ④NH4Cl ⑤NH4Al(SO4)2 ⑥(NH4)2SO4 ,其中c(NH4+)从大到小的排列顺序为______________(填序号)。
(4)已知下列四组溶液中:①Na2S ② H2S 和NaHS ③H2S ④NaHS ,每种溶质的物质的量浓度均为0.4 mol·L-1,回答下列问题:
c(H2S)从大到小的顺序为____________________________(填序号)
c(S2-)从大到小的顺序为_____________________________(填序号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com