
 2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。
2C(g) 经2分钟反应达到平衡,此时生成0.2mol C。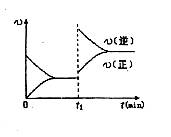
 2C(g)
2C(g)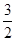 V(C)=
V(C)= 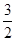 ×(0.2÷2)÷2 =" 0.075" mol.L-1.min-1
×(0.2÷2)÷2 =" 0.075" mol.L-1.min-1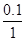
 100% =" 10%"
100% =" 10%" 

科目:高中化学 来源:不详 题型:单选题
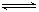 PCl3(g)+Cl2(g),反应达到平衡时,PCl3在混合气体中的体积分数为m%,保持温度和容积不变,再加入1mol PCl5,反应达到平衡时,PCl3在混合气体中的体积分数为n%,则m和n的关系正确的是( )
PCl3(g)+Cl2(g),反应达到平衡时,PCl3在混合气体中的体积分数为m%,保持温度和容积不变,再加入1mol PCl5,反应达到平衡时,PCl3在混合气体中的体积分数为n%,则m和n的关系正确的是( )| A.m > n | B.m < n |
| C.m = n | D.无法比较 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2 SO3反应。进行到4mi n时,测得SO2为0.4mol,若反应进行到2min时,容器中的SO2为( )
2 SO3反应。进行到4mi n时,测得SO2为0.4mol,若反应进行到2min时,容器中的SO2为( )| A.1.6mol | B.1.2 mol | C.大于1.6 mol | D.小于1.2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)的下列叙述中,能说明反应已达到平衡的是( )
2C(g)的下列叙述中,能说明反应已达到平衡的是( )| A.单位时间内消耗amolA,同时生成2amolC |
| B.C生成的速率与C的分解速率相等 |
| C.若容器体积不变,容器内的压强不再变化 |
| D.混合气体的物质的量不再变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向反应体系中加入催化剂以加快化学反应速率 |
| B.温度越高,化学反应速率越快 |
| C.由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深 |
| D.温度越高, 工业合成氨的产率越低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g);△H<0 。
2NH3(g);△H<0 。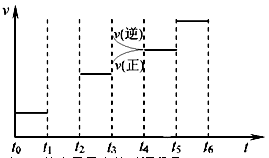
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NO2(g)△H=" +57" kJ·mol-1,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g)△H=" +57" kJ·mol-1,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4)/mol | 0.40 | a | 0.20 | c | d | e |
| n(NO2)/mol | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com