
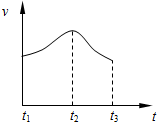
 �ѳ�ȥ����Ĥ��þ��Ͷ�뵽ʢ��ϡHCl���Թ��У������������������ʱ仯�����ͼ��ʾ��
�ѳ�ȥ����Ĥ��þ��Ͷ�뵽ʢ��ϡHCl���Թ��У������������������ʱ仯�����ͼ��ʾ������ ��þ����ķ�ӦΪ���ȷ�Ӧ����Ӧ��ʼʱ���¶Ȳ������ߣ���Ӧ�������������ŷ�Ӧ�ļ��ԣ���Ӧ���Ũ�����ͣ���ʱŨ�ȵ�Ӱ������¶ȵ�Ӱ�죬��Ӧ���ʷ�����С���Դ˽����⣮
��� �⣺��1��þ�����ᷴӦ�����Ȼ�þ����������Ӧ�����ӷ���ʽΪMg+2H+=Mg2++H2�����ʴ�Ϊ��Mg+2H+=Mg2++H2����
��2������þ������ķ�Ӧ�������Կ���߷�Ӧ���ٶȣ�t1��t2�ٶȱ仯������Ҫԭ���Ƿ�Ӧ����ʹ��Һ�¶����ߣ��ʴ�Ϊ��þ��������ķ�Ӧ�Ƿ��ȷ�Ӧ����Һ�¶����ߣ���Ӧ���ʼӿ죻
��3��t2��t3�ٶȲ��ϱ���������Ϊ������������������þ�Լ���Һ�е��Ȼ�����Ӧ�����IJ��ϱ��٣����·�Ӧ�ٶȱ�����
�ʴ�Ϊ������Ũ�ȼ�С����Ӧ���ʼ�����
��4�������������������ʣ��ɽ������Ũ�Ȼ��������������ֻ��AD���ϣ��ʴ�Ϊ��AD��
���� ���⿼��Ӱ�컯ѧ��Ӧ���ʵ����أ�Ϊ��Ƶ���㣬�����¶ȡ�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�켰ͼ�����Ϊ���Ĺؼ���ע�ط�����֪ʶӦ�������Ŀ��飬��Ŀ�ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��H
��H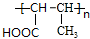 ��
�� +2Cu��OH��2$\stackrel{��}{��}$
+2Cu��OH��2$\stackrel{��}{��}$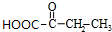 +Cu2O+2H2O��E��F2
+Cu2O+2H2O��E��F2 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$ +2H2O��
+2H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ƿ���������һ�������ɸ�CH2ԭ���ŵ����ʣ��˴�һ����ͬϵ�� | |
| B�� | ����ʽΪC5H12O�����������ܷ���������Ӧ�Ĵ���6�� | |
| C�� | 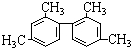 ������������11��̼ԭ�Ӵ���ͬһƽ�� ������������11��̼ԭ�Ӵ���ͬһƽ�� | |
| D�� | 1mol ��-������ͪ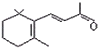 ��1mol H2�����ӳɷ�Ӧ�ɵõ�3�ֲ�ͬ���� ��1mol H2�����ӳɷ�Ӧ�ɵõ�3�ֲ�ͬ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl�ĵ���ʽΪ 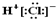 | B�� | N2�Ľṹʽ N��N | ||
| C�� | Oԭ�Ӵ��ڻ�̬�Ĺ����ʾʽ��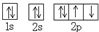 | D�� | �õ���ʽ��ʾMgCl2���γɣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
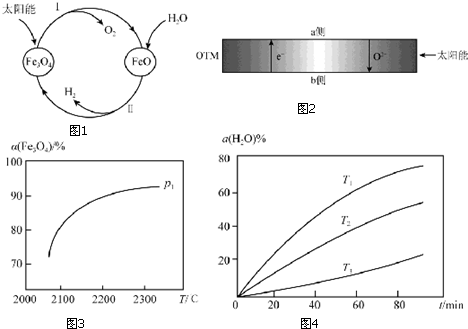
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 1 mol H2O�����е�ԭ����Ϊ3NA | |
| B�� | ���³�ѹ�£�32g O2���е���ԭ����Ϊ2NA | |
| C�� | 11.2L����������ԭ����ΪNA | |
| D�� | 0.1mol•L -1NaCl��Һ��c��Na+��Ϊ0.1 mol•L -1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com